Sumario
Haga click en los siguientes links para ir directamente a las clases de este capítulo:
- Clase 1
- Clase 2
- Clase 3
- Clase 4
- Clase 5
- Clase 6
- Clase 7
- Clase 8
- Clase 9
- Clase 10
- Clase 11
- Clase 12
- Clase 13
- Clase 14
- Clase 15
- Clase 16
- Clase 17
- Clase 18
3.1.1 El corazón como bomba.
3.1.2 Características de las fibras musculares cardiacas.
3.1.3 Diferencia con el musculo esquelético.
3.1.4 Potencial de acción tipo meseta (grafico)
3.1.5 Periodo refractario.
El corazón adulto pesa alrededor de 250 a 300 gr (Vacío). Está compuesto de 4 cavidades:
2 cámaras de cebamiento y 2 cámaras de eyección.
Las cámaras de cebamiento son las aurículas que se encargan de acumular sangre proveniente de los grandes troncos venosos y con una ligera contracción, completar el llenado ventricular.
Los ventrículos, de paredes más potentes son los encargados de enviar la sangre hacia la circulación pulmonar (ventrículo derecho) y a la circulación sistémica o periférica el ventrículo izquierdo.
A la aurícula derecha le llega la vena cava superior con sangre con hemoglobina desoxigenada de la mitad superior del cuerpo , la vena cava inferior con la válvula de Eustaquio que trae sangre de la mitad inferior del cuerpo , y por último el seno venoso coronario con su válvula de tebecio que trae sangre proveniente de las paredes cardiacas.
De la aurícula derecha este volumen de sangre pasa a través de la válvula tricúspide al ventrículo derecho que la expulsa hacia la arteria pulmonar para ser oxigenada a nivel del complejo alveolo capilar pulmonar. En su inicio la arteria pulmonar es anterior con relación a la aorta, pero después de un corto trayecto dirigiéndose hacia arriba y atrás se ubica en posición posterior al cayado aórtico.
La sangre proveniente de los alveolos pulmonares, regresa con hemoglobina saturada de O2 a través de 4 venas 2 de cada pulmón que desembocan todas en la pared posterior de la aurícula izquierda. Este volumen cruza la válvula mitral hacia el ventrículo izquierdo que la inyecta en la arteria aorta para ser distribuida en todo el organismo. Al inicio de la aorta se encuentran los senos de valsalva con los orificios de entrada de la coronaria izquierda y derecha en posición distal a las hojuelas valvulares.
A pesar que las 2 cavidades derechas y las 2 cavidades izquierdas están unas junto a las otras, la circulación del adulto normal no es en paralelo sino en serie, podemos decir una estructura delante de la anterior y antes de la siguiente.
Microscópicamente
El músculo cardiaco tiene características de músculo esquelético pero también de músculo liso. Con referencia al músculo esquelético, al igual que este, está formado por sarcomeras, pero solo tiene una triada en cada segmento por lo que la contracción del músculo cardiaco es más lenta. En cambio el músculo esquelético que tiene 2 triadas por sarcomeras tiene una contracción más rápida. Además el músculo cardiaco no tiene huso muscular.
En cuanto a la trasmisión del impulso nervioso, el miocardio se parece más al músculo liso sincitial, porque no utiliza trasmisor químico sino que el impulso se desplaza de membrana a membrana mediante trasmisión efáptica, no sináptica. Por tanto el impulso eléctrico pasa de fibra cardiaca a fibra cardiaca por contacto de sus membranas.
Contracción del músculo cardiaco
El potencial de acción que se irradia por el músculo cardiaco, ingresa de la misma forma que el músculo esquelético por los túbulos T produciendo el desplazamiento de los iones de calcio desde las cisternas para unirse con la Troponina C en forma análoga al músculo esquelético. Pero existe otra diferencia: el músculo esquelético no requiere de calcio extracelular para su contracción, pero el músculo cardiaco no le basta el calcio intracelular sino que requiere de una cantidad adicional que ingresa durante la fase 2 de la Repolarización del potencial de acción tipo meseta esto se consigue por túbulos T muchos más voluminosos que los del túbulo esquelético.
Duración del proceso mecánico (contracción)
El tiempo de duración de la contracción del músculo cardiaco es de alrededor de 0.2 a 0.3 segundos en el músculo ventricular pero su potencial de acción (evento eléctrico) es muy prolongado, de tal forma que cuando la membrana muscular cardiaca sale de periodo refractario, el músculo cardiaco ya se encuentra en proceso de relajación avanzado.
De esta forma solo acepta un nuevo impulso eléctrico casi en completa relajación, por lo que es imposible tetanizarlo.
En cambio el músculo esquelético con potencial de acción corto tipo espiga, que termina rápido, membrana puede aceptar un nuevo estimulo antes que la relajación muscular se inicie, de esta forma estímulos repetitivos producen contracción tetánica del musculo esquelético.
|
Musculo esquelético |
Musculo cardiaco |
|
1.-multinucleado |
Mononucleado |
|
2.- retículo endoplasmatico mas desarrollado (forman triadas se encuentran en líneas Z) |
Retículo endoplasmatico menos desarrollado (formas diadas en las uniones A-I) |
|
3.-Tienen formas fusiforme |
Tienen forma rectangular |
|
4.-impulso nervioso originado en la placa terminal |
Impulso nervioso se origina en el nodo sinoauricular |
|
5.-se tetaniza |
No se tetaniza |
|
6.-la contracción es mas rápida y menos prolongada |
Posee una contracción menos rápida y mas prolongada |
|
7.- su fuente de energía es la glucosa |
Su fuente de energía es la glucosa, ácidos grasos y lactato. |
|
8.-potencial de acción tipo espiga |
Potencial de acción tipo meseta |
|
9.- esta inervado por los nervios raquídeos |
Inervación simpática y parasimpática |
Debemos recordar que el potencial de acción del musculo cardiaco es de tipo meseta.
El gráfico del potencial de acción tipo meseta revela ciertas particulares de la Repolarización que no se observan en el potencial de acción tipo espiga por la gran velocidad en la que se realiza.
La despolarización o fase cero es igual en los 2 tipos de potencial de acción pero en el potencial de acción tipo meseta se observan 4 etapas o fases de la Repolarización:
Fase 1.-Se inicia en el sobretiro se cierran los canales de Na y se abren los canales de salida de K pero muy limitadamente con lo que el gráfico realiza un pequeño descenso en dirección a la línea isoeléctrica.
Fase 2.- por motivos desconocidos se cierran los canales de salida de potasio y se activan los llamados canales lentos de Na* y Ca** que producen la entrada de cargas positivas durante muchos milisegundos. Esto mantiene a la superficie interior de la membrana cargada positivamente por encima de la línea isoeléctrica, graficándose una línea casi horizontal que es lo que se conoce como meseta del potencial de acción. Las células ventriculares del miocardio son las que tienen la meseta más prolongada, alrededor de 250 milisegundos (msg).
Fase 3.- al final de la meseta se cierran los canales lentos de sodio y calcio con lo que finaliza la entrada de cargas positivas, se abren bruscamente una gran cantidad de canales para la salida de potasio con la consiguiente pérdida de cargas positivas. La superficie interior de la membrana se torna progresivamente negativa, el gráfico cruza la línea isoeléctrica en dirección al valor del potencial de membrana pasando por la línea que representa el nivel umbral.
Este momento se conoce como el periodo súper normal. Cuando analizamos el perfil electrocardiográfico corresponde a la rama descendente de la onda T si en este sitio se aplica un estímulo, la membrana es muy vulnerable y puede producirse un caos eléctrico en las células ventriculares (fibrilación ventricular) que es muy peligrosa.
La salida de potasio da lugar a que la electronegatividad interior alcance el nivel de potencial de reposo (-90 milivoltios) pero no se detiene ahí llegando hasta un nivel más negativo que el potencial de reposo, alrededor de -100 milivoltios. Este estado se conoce con el nombre de Hiperpolarización, para poder aplicar un estímulo que lleve a nivel umbral se debe incrementar la intensidad. Una membrana hiperpolarizada es más difícil de estimular que cuando su negatividad es de -90 milivoltios.
Fase 4.- al final de la Hiperpolarización se cierra los canales de salida de ión de potasio y se abren canales lentos de entrada de sodio. Cada vez que entra un ión de sodio disminuye la electronegatividad interior. Cuando se alcanza el nivel de reposo se cierra estos canales espontáneamente.
La fase 4 no es igual para todas las células excitables en la mayoría termina la entrada de sodio cuando se alcanza el potencial de reposo. Pero existe un grupo de células excitables llamadas automáticas en las cuales la fase 4 no se detiene en nivel de reposo sino que sigue entrando sodio a una lenta velocidad disminuyendo la negatividad de -90 a -89 a -88 y así sucesivamente hasta llegar a nivel umbral – 57 con lo que se desencadena otro potencial de acción sin que haya estímulo alguno.
Estas células automáticas se encuentran en el nódulo auriculoventricular, el haz de His, las ramas de Purkinje y hasta en las propias células ventriculares.
Esta fase 4 de las células automáticas se conoce con el nombre de despolarización diastólica.
Cada célula automática tiene un número determinado de despolarizaciones diastólicas por minuto, de acuerdo a la velocidad de entrada de sodio.
La mayor frecuencia por minuto la posee el nódulo sinoauricular con 75 x min siguiendo en orden decreciente el nódulo auriculoventricular con 60 x min, el haz de His 45 x min, las ramas de Purkinje 30 x min y por último las fibras musculares ventriculares 15 x min aproximadamente.
El nódulo sinoauricular se lo conoce con el nombre de marcapaso fisiológico por poseer el mayor número por despolarización por minuto que los otros tejidos automáticos.
Periodo refractario
La membrana de una célula excitable no puede aceptar otro estímulo hasta que haya finalizado el potencial de acción (despolarización más Repolarización) anterior este tiempo se llama periodo refractario, que es muy variable entre las diferentes células.
Las neuronas y el músculo esquelético tienen periodo refractario muy cortos porque su potencial de acción dura unas pocas msg. En cambio el músculo cardiaco especialmente las células ventriculares tienen un potencial de acción muy prolongado. Esto es lo que impide que el músculo cardiaco se tetanice pues la secuencia es la siguiente:
Despolarización- contracción muscular-relajación muscular-Repolarización.
Esto significa que la despolarización obligatoriamente produce contracción muscular cardiaca, pero como el potencial de acción es muy prolongado no puede transmitir un nuevo impulso por estar en periodo refractario, mientras tanto la relajación del musculo cardiaco se produce porque ella no depende de la repolarización si no de la disponibilidad de ATP.
En cambio el músculo esquelético si puede tetanizarse porque tiene un periodo refractario muy corto de modo que cuando su membrana puede aceptar otro estímulo todavía no se ha producido la relajación muscular, de tal forma que estímulos repetitivos pueden prolongar la contracción en forma indefinida y nunca permitir que el músculo se relaje.
|
EN RESUMEN: EL MÚSCULO ESQUELÉTICO PUEDE TETANIZARCE. EL MÚSCULO CARDIACO NUNCA SE TETANIZA. |
3.2.1 El ciclo cardiáco
3.2.2 Divisiones de la sístole y de la diástole
3.2.3 Duración de cada una en relación con la frecuencia cardiaca
3.2.4 Sístole ventricular; contracción isométrica; periodo de eyección; relajación isométrica.
3.2.5 Diástole y sus periodos.
3.2.6 Bradicardia y Taquicardia.
CICLO CARDIÁCO
El corazón es una bomba aspirante- impelente. La contracción del músculo cardiaco produce un acortamiento de sus fibras que disminuye el volumen interior de sangre que se ve forzada a salir. Un sistema de válvulas hace que el volumen sanguíneo vaya primero de aurículas a ventrículos y de ventrículos a las grandes arterias.
Analizaremos primero el ciclo cardiaco desde el punto de vista del ventrículo izquierdo, que es la cavidad más gruesa y fuerte del corazón y encargada de hacer circular la sangre por todo el cuerpo a excepción de la circulación pulmonar de la cual se encarga el ventrículo derecho.
El ciclo cardiaco consta de dos partes SÍSTOLE y DIÁSTOLE.
La sístole contracción y expulsión y la diástole relajación y llenado de sus cavidades.
Ambos procesos son activos y con gasto de energía. Antiguamente se pensaba que solamente la sístole era activa y que la diástole era pasiva y que como la diástole normalmente es más duradera que la sístole se llegó a pensar antiguamente que el corazón era un órgano poco trabajador que descansaba más del tiempo que estaba en actividad.
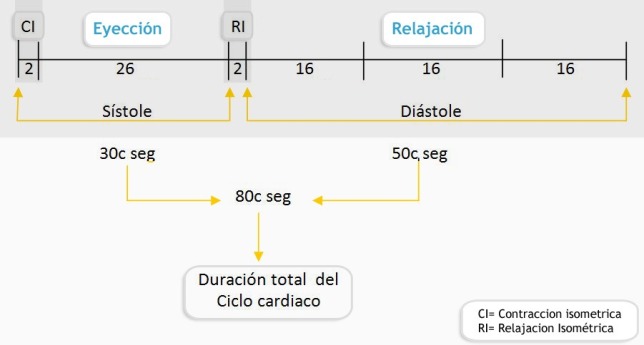
La duración total del ciclo cardiaco depende de la frecuencia cardiaca por minuto.
Estando en relación inversa con ella a mayor frecuencia la duración del ciclo es menor y a menor frecuencia la duración del ciclo es más prolongada. Pero la diástole es la que sufre mayor alteración que la sístole.
A la frecuencia de 75 x min el ciclo cardiaco total es de 80 centésimas de seg correspondiendo a la sístole 30 centésimas y la diástole 50 centésimas de seg.
SÍSTOLE VENTRICULAR
La sístole consta de tres fases: contracción isométrica, periodo de eyección y relajación isométrica con una duración de 2-26-2 seg respectivamente total 30 seg si la frecuencia cardiaca es de 75 min.
Contracción isométrica o isovolumétrica
en este momento el músculo cardiaco aumenta su tensión pero todavía no hay acortamiento de las fibras. Un ejemplo seria si flexionamos el antebrazo en ángulo recto con respecto al brazo, si ponemos un peso de varios kilogramos en la mano y no queremos que el antebrazo se mueva tenemos que poner en tensión al músculo bíceps sin que variara su longitud. Si lo palpamos notaremos una mayor dureza muscular.
A nivel microscópico, lo que sucede en la contracción isométrica es que las cabezas de los puentes cruzados que pertenecen a los filamentos gruesos, se han unido a los sitios activos de ADP que se encuentran en los filamentos delgados, pero todavía no se ha producido el desplazamiento (golpe activo) de los filamentos.
Si nos ubicamos imaginariamente dentro de la cavidad ventricular izquierda que está llena en su totalidad (volumen de fin de diástole) la sangre al tratar de regresarse a la aurícula izquierda cierra las válvulas aurículo ventriculares (mitral), pero todavía no se han abierto las válvulas semilunares (aórtica). Sucede lo mismo en el ventrículo derecho se cierra la tricúspide pero todavía no se ha abierto la válvula semilunar pulmonar esto quiere decir que durante la contracción isométrica, 2 cseg las 4 válvulas cardiacas están cerradas.
Al inicio de la contracción isométrica el cerramiento de la mitral y tricúspide, más la puesta en tensión de los pilares tendinosos que la sostienen produce vibraciones conocidas como primer ruido cardiaco.
PERIODO DE EYECCIÓN
Se inicia con el acortamiento de las sarcomeras ventriculares, sube la presión intracavitaria ventricular izquierda hasta alrededor de 120 mmHg, superando la presión que existía en ese momento en la arteria aorta, lo cual abre la válvula semilunar. Debemos de recordar que normalmente las aperturas valvulares son silenciosas y que solo los cerramientos valvulares son los que producen ruidos cardiacos.
El periodo de eyección dura aproximadamente 26 seg estando el punto máximo de la curva de presión ventricular en la mitad de este tiempo o sea 13 seg, a partir del cual la presión intracavitaria ventricular comienza a descender cayendo por debajo de la presión que existe en la aorta.
RELAJACIÓN ISOMÉTRICA
Es todo lo contrario que la contracción isométrica. En este periodo disminuye la tensión del musculo pero todavía no se ha producido un alargamiento de su longitud.
Microscópicamente lo que sucede es que se han separado las cabezas de los puentes cruzados de los filamentos gruesos de los sitios activos de ADP que se encuentran en los filamentos delgados, pero todavía no se ha producido un aumento de longitud de la sarcomera, el tiempo es de 2cseg (0,02seg) .
Al iniciarse la relajación isométrica la presión en la aorta supera a la de la cavidad ventricular izquierda, y el retroceso de la sangre cierra la válvula semilunar, pero todavía no se ha abierto la válvula mitral. Lo mismo sucede en el ventrículo derecho la sangre que trata de regresar de la arteria pulmonar cierra la válvula semilunar, pero todavía no se ha abierto la válvula tricúspide.
De esta manera otra vez durante el ciclo cardiaco se vuelve a presentar el cerramiento de las 4 válvulas al mismo tiempo. El cerramiento de las válvulas aórticas y pulmonar en ese orden, producen vibraciones que se conocen con el nombre de segundo ruido cardiaco. Ocurren al inicio de la relajación isométrica
DIÁSTOLE
Es la etapa de relajación ventricular, comprende 3 periodos:
1.-Periodo de llenado rápido o protodiástole. De aproximadamente de 16 a 17 seg representa el 50% del llenado ventricular, debido a que durante la sístole, estando cerradas las válvulas auriculo ventriculares, la sangre proveniente de las cuatro venas pulmonares se acumuló en la aurícula izquierda. Lo mismo sucedió en la aurícula derecha, donde se acumuló sangre proveniente de las venas cavas superiores, inferiores y del seno coronario.
Al iniciarse la protodiástole la apertura de la mitral y tricúspide envía el volumen de sangre acumulada en las aurículas al ventrículo correspondiente.
2.-Periodo de diastasis, periodo de llenado lento o mesodiástole. Mientras se encuentran abiertas las válvulas A-V con sus velos valvulares separados, la sangre proveniente de las cuatro venas pulmonares pasa directamente al ventrículo izquierdo. De igual manera la sangre proveniente de las venas cavas pasa directamente al ventrículo derecho.
El termino diastasis, proviene del griego antiguo y significa “separación de estructuras”. También se lo utiliza en una patología de la estructura de la pared abdominal, cuando los músculos rectos anteriores no están unidos en la línea central, y cuando la persona hace un esfuerzo, se produce una protusión entre los dos músculos en forma de quilla de barco. Esto se conoce como diastasis de los rectos abdominales. Al igual que el periodo anterior y el que le sigue tiene una duración de 16 a 17 seg, y representa el 20% del llenado ventricular
3.- Periodo de contracción auricular, teledíastole o presístole. Es la parte final de la diástole ventricular, de igual duración que los anteriores de 16 a 17 seg, representa el 30% restante del llenado ventricular. Durante este periodo al contraerse las aurículas completan el llamado volumen de fin de diástole.
En caso de parálisis auricular este 30% no se efectúa, por la incapacidad de contracción de las aurículas. El paciente con esta afección puede mantenerse asintomático mientras se encuentra en estado de reposo, porque su corazón se contrae con el 70% del volumen de llenado.
Pero al pasar del reposo al ejercicio físico, el corazón requiere el 100% de su llenado, la aurícula no se lo puede proveer por estar paralizada y no existir contracción auricular. En este caso aparecen síntomas como debilidad, mareos, sudoración, y taquicardia.
En un caso completamente diferente, si la válvula mitral presenta estenosis (la válvula no puede abrirse completamente) la contracción auricular tratando de hacer pasar un volumen de sangre a través de un orificio estrecho, produce un torbellino que da lugar a vibraciones llamadas soplo de estenosis mitral o presistolico que se lo ausculta al final de la diástole.
Se llama presistolico porque aparece justo antes que comience la sístole del siguiente ciclo cardiaco
BRADICARDIA Y TAQUICARDIA
La frecuencia cardiaca promedio en la especie humana, en estado de reposo es de 75 x min, con un límite inferior de 60 y un límite superior de 100.
En caso de frecuencia cardiaca menor de 60 x min se conoce con el nombre de bradicardia, cuando la frecuencia cardiaca es mayor de 100 se conoce como taquicardia.
3.3.1 Curva de volumen ventricular
3.3.2 Concepto de volumen de fin de diástole
3.3.3 Volumen de fin de diástole
3.3.4 Volumen sistólico
3.3.5 Fracción de eyección
3.3.6 El corazón hipo eficaz e híper eficaz
3.3.7 Concepto de insuficiencia cardiaca.
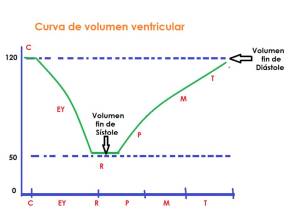
Recordemos que el estudio de la función cardiaca siempre tiene como punto de referencia a la actividad ventricular izquierda.
El volumen de sangre varía de acuerdo al momento del ciclo cardiaco. El nivel máximo de sangre que contiene el ventrículo izquierdo ocurre al final de la diástole. Debemos notar que el ventrículo en ningún momento se queda vacío, pues obedeciendo a leyes fundamentales de las cavidades esféricas, y teniendo la sarcomera solo un porcentaje de acortamiento máximo (25%), durante la máxima acortación quedara siempre un remanente sanguíneo en su cavidad que se conoce con el nombre de fin de sístole. En un corazón de aproximadamente 300 gr de peso el volumen de fin de sístole es de alrededor de 50 ml.
Al iniciarse la diástole, durante la protodiastole este volumen aumenta, continua ingresando sangre proveniente de las venas pulmonares durante la meso diástole, y se completa el llenado durante la tele diástole, llegando en un corazón de tamaño normal a 120 ml que es lo que se conoce con el nombre de volumen de fin de diástole.
La diferencia entre el volumen de fin de diástole y el volumen de fin de sístole se conoce con el nombre de volumen sistólico y representa la cantidad neta de sangre que es inyectada por el ventrículo izquierdo en la arteria aorta.
En el caso del volumen ventricular, las mismas cifras se aplican para el ventrículo derecho y el ventrículo izquierdo pues manejan volúmenes bastantes similares. No es el mismo caso de la curva de presión ventricular en que las fuerzas que se generan son muy diferentes para cada ventrículo.

CI: Contración isométrica.
Período de eyección.
R.I : Relajación isométrica
Fracción de eyección.
Debido a que las variaciones en la estatura de personas adultas de las diferentes razas de la especie humana por ejemplo los indígenas de la región interandina que pueden tener una estatura de 1,20 cm, en cambio podemos encontrar individuos de origen africano que miden 2,15 cm de estatura en lo cual hace que el tamaño de su corazón también sea muy variable. Un volumen sistólico de 70 ml podría ser excelente para una persona de baja estatura pero sería insuficiente para una persona de más de 2 m de alto. De tal manera es mejor hablar en cifras porcentuales en vez de cifras absolutas.
Por este motivo se ha diseñado lo que se llama fracción de eyección que consiste en determinar cuál es el porcentaje del volumen de fin de diástole que se inyecta en la arteria aorta durante la sístole.
Formula:
El valor normar debe ser mayor del 55 %.
Pero una disminución de menos de 50% nos indica una insuficiencia cardiaca, estado en el cual el corazón no es capaz de cumplir satisfactoriamente su función de bomba.
Si la fracción de eyección es de alrededor de 40%, la insuficiencia cardiaca es grave y en casos de fracción de eyección de alrededor de 25% se considera un estado premortem.
El corazón hipoeficaz e hipereficaz
El corazón de los atletas genéticamente diseñado para esfuerzos muy prolongados, los corredores de maratón tienen una fracción de eyección por encima de 75% esto es lo que se llama corazón hiper eficaz.
En cambio si la fracción de eyección es menor de 55% se trata de un corazón hipo eficaz.
Concepto de insuficiencia cardiaca
Es un estado patológico relacionado con la incapacidad del corazón de eyectar toda la sangre que le llega por la venas es decir un corazón hipo eficaz.
En ciertas ocasiones falla uno de los 2 ventrículos pudiendo tratarse por tanto de insuficiencia cardiaca izquierda e insuficiencia cardiaca.
Si el ventrículo izquierdo falla se produce congestión en el sistema vascular pulmonar , si es el ventrículo derecho que esta insuficiente la congestión se presenta en el territorio de la vena cava inferior, especialmente a nivel hepático que aumenta de tamaño y es muy doloroso
( hepatomegalia dolorosa) palpable por debajo del reborde costal derecho.
3.4.1 Curva de presión ventricular
3.4.2 Curva de presión aortica
3.4.3 Curva de presión auricular
3.4.4 Fono cardiograma
3.4.5 El perfil electrocardiográfico
CURVA DE PRESIÓN VENTRICULAR
Reiteramos nuestra posición imaginaria dentro de la cavidad ventricular izquierda, la cual va a experimentar grandes variaciones de presión de acuerdo al momento del ciclo cardiaco. A diferencia de la curva de volumen ventricular, que es prácticamente igual para ambos ventrículos, la curva de presión es diferente para el ventrículo izquierdo y derecho. El ventrículo izquierdo tiene paredes más gruesas y por tanto puede desarrollar mayor tensión que el ventrículo derecho de paredes más delgadas. Durante la contracción isométrica aumenta enormemente la tensión desde 0 mmHg hasta alrededor de 120 mmHg en el punto medio del periodo de eyección, lo suficiente mayor que la presión en la arteria aorta con lo cual se abre la válvula semilunar.
Esto ocurre aproximadamente cuando ha trascurrido 2+13 seg. El 2 corresponde a la duración de la contracción isométrica y el 13 es la mitad de la duración del periodo de eyección. Total 15 cseg.
Inmediato a esto la tensión dentro de la cavidad ventricular disminuye tan rápido como subió. Cuando comienza la relajación isométrica a la final de la sístole la presión cae a 0 dentro de la cavidad ventricular.
El llenado ventricular durante las tres fases de la diástole puede incrementar ligeramente la presión ventricular izquierda pero nunca más de 20 mmHg que es el límite máximo de la presión diastólica ventricular izquierda.
En el caso del ventrículo derecho que tiene paredes más delgadas solamente desarrolla presiones máximas sistólicas de hasta 30 mmHg lo que representa solo una cuarta parte de la presión que desarrolla el ventrículo izquierdo.
Debemos recordar que la relajación diastólica es un proceso activo y que en caso de no realizarse satisfactoriamente aumentaría el valor de la presión intracavitaria, al final de la diástole, por encima de 20mmHg.
CURVA DE PRESIÓN AORTICA
Durante toda la diástole la presión intra aórtica se mantiene en alrededor de 80mmhg, esto es lo que se denomina presión diastólica o mínima.
Al inicio de la sístole ventricular, cuando la presión ventricular supera la presión aórtica, se abre la válvula semilunar y penetra en la aorta ascendente un volumen de sangre que aumenta la presión dentro de la arteria. A mitad de la sístole, cuando han transcurrido 15 cseg, se alcanza el nivel máximo de presión intra aortica, llamada presión sistólica, o máxima, esta se encuentra en alrededor de 120 mmHg.
Inmediatamente, debido a la elasticidad de la pared arterial, se forman dos ondas de sangre, una que progresa hacia la periferia para perfundir los órganos y otra onda, que trata de regresarse hacia el ventrículo izquierdo.
Debido a las características anatómicas de las tres hojuelas valvulares, se cierra la válvula aortica, produciendo una muesca en la rama descendente de la curva de presión aórtica, generalmente en el tercio superior. Esta deflexión se conoce con el nombre de incisura dicrota y marca el cerramiento valvular aórtico.
CURVA DE PRESIÓN AURICULAR
Las presiones dentro de las aurículas son mucho menores que en los ventrículos siendo la presión en la aurícula izquierda (2 a 4 mmHg) ligeramente superior que la de la aurícula derecha (0 a 2 mmHg) cuando la persona está en decúbito dorsal (horizontal).
Esta ligera diferencia entre aurícula izquierda y aurícula derecha que se inicia de inmediato al nacimiento del individuo es lo que contribuye a que el septum primiun se adose al agujero oval en el tabique interauricular, impidiendo el paso de sangre de la aurícula izquierda a la aurícula derecha.
Se han descrito 3 ondas en la curva de presión auricular, pero que son muy ligeras en cuanto a intensidad:
Onda A que representa la contracción auricular al final de la diástole ventricular.
Ondas C que se inscriben durante la contracción isométrica y se debe a la protusión del aparato valvular auriculo ventricular hacia las aurículas durante su cerramiento.
Onda V representa un ligero incremento de la presión intraauricular por aumento de su volumen mientras se encuentran cerradas las válvulas auriculo ventriculares, debido a que la sangre de los sistemas venosos llega ininterrumpidamente a las aurículas
FONOCARDIOGRAMA
Consiste en el registro gráfico de las vibraciones producidas en las cavidades cardiacas y en los aparatos valvulares. Debemos recordar que solo los cerramientos valvulares producen ruido y que normalmente las apreturas valvulares normales son silenciosas.
 |
La circulación de la sangre por las cavidades cardiacas y por los vasos sanguíneos se realiza por un mecanismo llamado laminar, que consiste en que las capas de sangre más exteriores circulan a una velocidad menor que las capas de sangre ubicadas en el centro del vaso sanguíneo, de modo que una capa actuaría como superficie de rodamiento de la más internas. Esto se conoce como flujo laminar y es silenciosa.
Cualquier obstáculo que exista en la pared del vaso o en los tabiques de las cavidades cardiacas dará lugar a un flujo turbulento, que producirá alteraciones conocidas con el nombre de soplos cardiacos.
El Fonocardiograma es un método en extinción, y solo se lo utiliza raramente en los laboratorios de fisiología.
El cerramiento de las válvulas auriculo ventriculares produce vibraciones de tonalidad baja o grave llamada primer ruido cardiaco.
El cerramiento de las válvulas semilunares produce vibraciones llamadas segundo ruido cardiaco.
En un corazón normal el Fonocardiograma solo registrara las vibraciones correspondientes al primero y segundo ruido. Cualquier otra vibración registrada significara una alteración.
EL PERFIL ELECTROCARDIOGRÁFICO.
Es el registro de la actividad eléctrica del corazón. Tradicionalmente se ha denominado a las deflexiones electrocardiográficas como ondas P-Q-R-S-T siguiendo el orden alfabético.
Las ondas que se inscriben hacia arriba de la línea isoeléctrica se las denomina positivas y las que se dirigen hacia abajo, se las llama ondas negativas.
Debemos recordar que para que se efectuara la contracción cardiaca, debe estar precedida de una despolarización. Por tanto antes de la contracción auricular debe haber una onda P que representa la despolarización de las aurículas.
Las ondas Q-R-S se las denomina en conjunto como complejo QRS, y representan la despolarización de los ventrículos como evento eléctrico previo a la contracción mecánica ventricular (sístole).
La onda T, representa a la repolarización de los ventrículos y se inscriben antes de la diástole ventricular.

3.5.1 Ley de Frank – Starlyng
3.5.2 Concepto de precarga y postcarga
3.5.3 El gasto cardiaco
3.5.4 Regulación simpática y parasimpática
3.5.5 Propiedades del corazón
3.5.6 Metabolismo energético del corazón
LEY DE FRANK – STARLYNG
“Dentro de los límites fisiológicos, el corazón es capaz de inyectar en las grandes arterias toda la sangre que le llega por las venas sin permitir un remanso en ellas”. El límite fisiológico es de 25 litros por minutos.
PRECARGA
Es el volumen de sangre que le llega por la vena cava superior e inferior a la aurícula y ventrículo derecho.
POSTCARGA
Es la dificultad que tiene el ventrículo izquierdo para inyectar la sangre en la arteria aorta y sus ramas. Esta dada por la resistencia periférica. A su vez la resistencia periférica esta en relación inversa al diámetro de las arteriolas que son vasos sanguíneos de menos de 100 micras de diámetro y que presentan en su capa media musculo liso inervado por el sistema nervioso simpático. Cuando se activa el simpático se produce una vasoconstricción arteriolar, disminuye el diámetro y aumenta la resistencia periférica.
Es el volumen de sangre que inyecta cada ventrículo en la arteria correspondiente.
Resulta de multiplicar el gasto o volumen sistólico por la frecuencia cardiaca.
El gasto sistólico en el normotipo es de alrededor de 70 ml, multiplicado por una frecuencia cardiaca de 75, da un gasto cardiaco de alrededor de 5000 ml de sangre por minuto.
Si aumenta la frecuencia cardiaca aumenta el gasto cardiaco pero hasta un cierto límite.
Cuando la frecuencia cardiaca es mayor de 140 x min el periodo de llenado diastólico es demasiado corto y siendo la sangre 3 veces más viscosa que el agua, el gasto cardiaco, comienza a disminuir progresivamente a medida que aumenta más la frecuencia, con frecuencias superiores a 200 x min el gasto cardiaco está en un nivel crítico y el paciente se pone pálido , sudoroso y frio, especialmente si no está en posición horizontal.
REGULACIÓN SIMPÁTICA Y PARASIMPÁTICA
El corazón es automático, pero su funcionamiento está regulado por el sistema nervioso autónomo. La inervación simpática se distribuye especialmente por la región del nodo sinoauricular y por los ventrículos, de modo que su actividad produce aumento de la frecuencia y de la fuerza de la contracción cardiaca.
Por el contrario el parasimpático se distribuye principalmente por las aurículas, nódo sinoauricular y auriculoventricular, cuya estimulación produce disminución de la frecuencia cardiaca y de la fuerza de contracción
PROPIEDADES DEL CORAZÓN
METABOLISMO ENERGETICO DEL CORAZON
El corazón es un “engúllelo todo “a diferencia del músculo esquelético que consume fundamentalmente glucosa, el músculo cardiaco en reposo consume fundamentalmente ácidos grasos y glucosa. Cuando entra en actividad máxima el corazón es capaz de utilizar como fuente de energía ácidos grasos, glucosa y ácido láctico en partes casi iguales. Esto es importante porque el ácido láctico es producto del metabolismo del músculo esquelético y el corazón es capaz de utilizarlo como fuente de energía en un verdadero proceso de reciclaje.
3.6.1 Sistema de excitación—conducción
3.6.2 El nódulo sino auricular como marcapaso fisiológico
3.6.3 Nódulo auriculo ventricular
3.6.4 Haz de His y sus ramas
3.6.5 Raíces de Purkinge
Sistema de Excitación – Conducción
El corazón tiene su propio sistema automático, llamado sistema de excitación-conducción, formado por nódulo sinoauricular, vías internodales: anterior, media y posterior, nódulo auriculo ventricular, haz de his y ramas de Purkinge.
Nodulo Sinoauricular
Situado en la parte superior de la aurícula derecha cerca de la desembocadura de la vena cava superior es el que posee mayor frecuencia de despolarización diastólicas por minuto, que en estado de reposo es de alrededor de 75 x min. Mayor que las otras células automáticas del corazón y por tanto se denomina marcapaso fisiológico. Recibe inervación simpática y parasimpática, casi por igual y por tanto reacciona a la estimulación simpática con aumento de su frecuencia, pero también a la parasimpática con disminución de la frecuencia.
Vías Internodales
Que conducen el impulso nervioso a una velocidad mayor de lo que sería conducido por las propias fibras auriculares.
Nodulo Aurículoventricular
Mejor llamado región del nódulo AV, porque está formado por tres tipos de fibras: fibras de transición – nodales propiamente dichas y fibras de unión. Está situado en la parte inferior de la aurícula derecha cerca del anillo fibroso de inserción de la válvula tricúspide. Mide aproximadamente de 3 a 5 mm de longitud y todas sus fibras tienen la característica de ser delgadas y no poseer cubierta de mielina, por lo que conducen a una velocidad de solo 5 cm x seg siendo probablemente las fibras de más baja velocidad de conducción. El objetivo es conseguir que el impulso nervioso sufra un retardo en su paso de aurículas a ventrículos antes de ingresar en el Haz de His.
Recordemos que la frontera entre aurículas y ventrículos está constituida por 2 anillos fibrosos de inserción de las válvulas auriculoventriculares (mitral y tricúspide) y que el único paso normal es a través de la región del nódulo AV hacia el Haz de His. Este retardo en la despolarización de los ventrículos, es de 10 centésimas de segundo. Y es lo que permite la contracción auricular para completar el llenado ventricular antes de iniciarse la sístole.
Pero en un pequeño porcentaje de personas, existe una vía aberrante de conducción entre aurículas y ventrículos, de tal modo que no existe este retardo y las aurículas y los ventrículos se contraen casi al mismo tiempo. Estas personas pueden en reposo estar asintomáticas, pero al pasar al ejercicio requiere un llenado completo ventricular, lo cual no se consigue y el paciente se torna pálido sudoroso y frio, pudiendo incluso perder el conocimiento.
Esto se conoce con el nombre de síndrome de pre excitación ventricular o Wolf- Parkinson – White. Una variante menos conocida se conoce como síndrome de Lown – Ganong – Levine y la diferencia entre uno y otro es la posición anatómica de las fibras de conducción aberrante.
Haz de His y Ramas de Purkinje
Es la vía común de conducción del impulso entre aurículas y ventrículos: un tercio de su longitud es intraauricular y los dos tercios restantes son intraventriculares, extendiéndose sobre la superficie izquierda del tabique interventricular.
En su extremidad distal se divide en rama izquierda y rama derecha llamadas ramas de Purkinje, que recorren la superficie endocardica en dirección al ápex de los ventrículos y luego se reflejan hacia arriba y atrás hasta cerca del borde posterior de los anillos fibrosos interventriculares.
La rama izquierda de Purkinje se divide en dos fascículos llamados izquierdo anterior e izquierdo posterior.
Raíces de Purkinje
Son prolongaciones transversales de las ramas de Purkinje que van de endocardio a pericardio cruzando el miocardio.
Debemos mencionar que el impulso nervioso tarda en despolarizar a las aurículas alrededor de 8 centésimas de segundo.
En cruzar la región del nódulo auriculoventricular 10 centésimas de segundo y en despolarizar los ventrículos 6 centésimas de segundo, extinguiéndose en las regiones posterobasales de ambos ventrículos, con un total de duración 24 centésimas de segundo.
3.7.1 Ruidos cardiacos
3.7.2 Componentes de los ruidos cardiacos
3.7.3 Ruidos cardiacos anormales; tercer y cuarto ruido cardiaco
3.7.4Focos de auscultación
3.7.5 Desdoblamiento fisiológico del segundo ruido en el foco pulmonar
3.7.6 El estetoscopio
RUIDOS CARDIACOS
Los ruidos cardiacos son vibraciones que se producen por el cerramiento de las hojuelas valvulares y las vibraciones de las cuerdas tendinosas y del anillo de sustentación valvular.
Recordemos que solo los cerramientos valvulares producen ruido y que las aperturas valvulares normales son silenciosas.
Normalmente se escuchan 2 ruidos cardiacos que se producen al comienzo y al final de la sístole durante la contracción isométrica el primer ruido y durante la relajación isométrica el segundo ruido.
Si la frecuencia cardiaca es de 75 x min entre el primero y el segundo ruido habrá alrededor de 26 cseg y se lo llama pequeño silencio.
Entre el segundo ruido y el primero del ciclo siguiente, transcurren alrededor de 50cseg y se lo ha llamado gran silencio.
El primer ruido cardiaco
Tiene dos componentes: mitral y tricuspideo.
Se cierra primero la válvula mitral por ser el sistema valvular que trabaja a mayor presión. Entre el cerramiento de la mitral y entre el cerramiento de la tricúspide transcurren 2 cseg, pero el sistema auditivo humano no puede diferenciarlo como dos ruidos separados a los dos componentes y lo escuchamos como un solo ruido.
El segundo ruido cardiaco
También tiene dos componentes: el aórtico y el pulmonar por el cerramiento de las válvulas semilunares respectivas. Se cierra primero la válvula aórtica y 2 cseg más tarde la válvula pulmonar que trabaja a menor presión, el oído humano tampoco puede reconocer estos 2 componentes como separados y lo percibimos como un ruido único.
Escala auditiva de la especie humana.
Los sonidos son vibraciones producidas por los objetos que dan lugar a ondas sonoras. La unidad se llama hertzio que significa una onda completa de sonido. La especie humana tiene una capacidad auditiva entre 20 y 20.000 hertzios, no puede escuchar sonidos de menos de 20 hertzios (infrasonidos), ni más de 20.000 hertzios (ultrasonidos).
Los sonidos de baja frecuencia se conocen como “bajos” o de tono grave como es el sonido del tambor.
Los sonidos de tonos altos “agudos”, son los que se parecen a los sonidos de una flauta.
El silbato para perros es un dispositivo que produce sonidos de frecuencia superior a 20.000 herzios no audible para la especie humana pero si para la especie canina.
Desdoblamiento Fisiológico del segundo ruido cardiaco en el foco pulmonar.
Normalmente el componente pulmonar del segundo ruido tiene un retraso de 2 cseg con respecto al componente aórtico, porque se cierra primero el sistema valvular que trabaja a mayor presión, pero el oído humano no lo reconoce como dos sonidos separados.
En el foco pulmonar sucede una situación especial, sobre todo en personas jóvenes y de tórax delgado. Esto ocurre al final de la inspiración, proceso durante el cual aumenta el retorno venoso, dando lugar a una prolongación del tiempo de eyección del ventrículo derecho con lo cual la diferencia entre el cerramiento de la válvula aórtica y el de la válvula pulmonar se incrementa a casi 4 cseg, en cuyo caso el oído entrenado los puede identificar como un sonido desdoblado.
La onomatopeya seria pumm – traak / pumm – traak / Inspiración.
Al final de la espiración, se produce el efecto contrario con lo cual el cerramiento de la válvula aórtica se retrasa, acercándose al de la válvula pulmonar.
La onomatopeya seria pumm – tak / pumm – tak / Espiración
FOCOS DE AUSCULTACION

Tercer ruido cardiaco
La pared ventricular, cuando es débil, por ejemplo posterior a un infarto, puede vibrar cuando la sangre proveniente del sistema venoso (4 venas pulmonares) cruza las válvulas aurícula ventriculares que están abiertas durante la meso diástole. Se produce un pequeño grupo de vibraciones justo en la parte media de la diástole ventricular dando lugar a un ruido de 3 tiempos llamado galope ventricular.
En cada ciclo cardiaco se escuchara por tanto el primer ruido luego el segundo ruido, seguido del tercer ruido cardiaco.
Entre el primero y segundo ruido habrá la normal separación de 26 centésimas de segundo, entre el segundo y el tercer ruido habrán 25 centésimas de segundo y entre el tercer ruido y el primero del ciclo siguiente existirá otras 25 centésimas de segundo.
Nótese que entre cada uno de los ruidos primero segundo y tercero se cronometrara un tiempo prácticamente igual si la frecuencia cardiaca es de 75 por minuto.
Cuarto ruido cardiaco
En ciertas ocasiones especialmente cuando existe hipertensión arterial sistémica, aumenta la presión en el ventrículo izquierdo, esto trae como consecuencia que la contracción auricular que completa el llenado ventricular al final de la diástole sea muy enérgica dando lugar a vibraciones que constituyen el cuarto ruido cardiaco. Esto se produce en el último tercio de la diástole o sea en la tele diástole, dando lugar a un ruido de 3 tiempos llamado galope auricular, la secuencia es:
Cuarto ruido —— primer ruido —— segundo ruido.
A la auscultación se puede reconocer porque el cuarto ruido está muy junto del primer ruido, precediéndolo con apenas 15 centésimas de segundo luego del primero viene el segundo después de 26 centésimas de segundo, seguido de un silencio de aproximadamente 35 centésimas de segundo que corresponde a la proto y meso diástole juntas.
· La onomatopeya seria para el galope ventricular: Pumm – Tak – Tak
· Y del galope auricular: Pum – Pumm – Tak.
También llamado fonendoscopio tiene 2 terminales
intercambiables mediante un giro de 180 grados. El primero tiene un diafragma
que sirve para atenuar y escuchar mejor los ruidos de alta frecuencia o de tono
agudo como es el segundo |ruido cardiaco , en cambio el otro terminal, llamado
campana no tiene diafragma y sirve para escuchar mejor los ruidos de tonos
bajos o graves como es el primer ruido
3.8.1 Electrocardiografía
3.8.2 Electrocardiógrafo
3.8.3 Derivaciones electrocardiográficas
3.8.4 representaciones esquemáticas de las derivaciones
3.8.5 los accidentes (ondas) del electrocardiograma
Electrocardiografía
La electrocardiografía es la técnica de registro gráfico de los potenciales de acción generados por el músculo cardiaco. El trazado que se obtiene, representa el registro de las variaciones de potencial eléctrico observados desde diferentes puntos de la superficie corporal, producidas por las fibras cardiacas en actividad. El aparato encargado de esto se conoce con el nombre de electrocardiógrafo.
El Electrocardiógrafo
Es un equipo diseñado para captar, procesar y graficar las débiles señales eléctricas generadas en el corazón. El electrocardiógrafo consta principalmente de 4 sistemas:
1. El sistema de electrodos
2. El amplificador electrónico.
3. El galvanómetro.
4. El sistema inscriptor.
1.- El Sistema de Electrodos
Los electrodos son placas metálicas que se aplican sobre la piel, para que exista un buen contacto entre estos dos elementos, la piel debe ser limpiada previamente con una solución alcohólica y una vez secada, se aplica entre ella y la placa, un gel conductor con el fin de disminuir la resistencia al paso de la corriente.
Las placas metálicas pueden tener diferentes formas, pero, todas están formadas por una aleación a partes iguales, 50% níquel – 50% plata. La señal eléctrica captada por los electrodos a nivel de la piel, es conducida por cables coaxiales hasta el amplificador.
2.- El Amplificador
El amplificador electrónico es un sistema diseñado para suministrar una “potencia” de salida, mucho mayor que la “potencia” de entrada y conducirla al galvanómetro.
3.- El Galvanómetro
Es el verdadero “cerebro” del electrocardiógrafo, se basa en las interacciones entre una corriente eléctrica y un imán. El mecanismo del galvanómetro está diseñado de forma que un imán permanente o un electroimán produce un campo magnético, lo que genera una fuerza cuando hay un flujo de corriente en una bobina cercana al imán.
El elemento móvil puede ser el imán o la bobina. La fuerza inclina el elemento móvil en un grado proporcional a la intensidad de la corriente. Este elemento móvil puede contar con un puntero o algún otro dispositivo que permita leer en un dial el grado de inclinación.
En el monitor cardiaco el galvanómetro responderá ante las variaciones de potencial amplificadas, dirigiendo los haces de electrones hacia arriba o hacia debajo de una línea horizontal llamada “línea isoeléctrica”, según el electrodo explorador “sienta” acercarse o alejarse la corriente proveniente del músculo cardiaco.
4.- El Sistema de Registro o Inscriptor
El papel electrocardiográfico.
Hasta hace algunos años, se utilizaba un papel de fondo negro, recubierto por una finísima capa de cera, que al ser derretida por el estilete caliente, conforme se movía el papel permitía observar el fondo, dibujando el llamado “perfil electrocardiográfico”. Actualmente, se utiliza un papel más específico en cuanto a la denominación “termo sensible”, pues la plumilla caliente, provoca en el papel una reacción química, dando lugar a un cambio de coloración (por ejemplo: papel rojo, trazado azul) va dibujando el perfil electrocardiográfico.
El electrocardiógrafo dispone de un pequeño motor eléctrico que haciendo mover un sistema de rodillos, permite el movimiento de la tira de papel.
La mayor parte de equipos, puede desplazar el papel a 2 velocidades: 25 mm x segundo ó 50 mm x segundo. Siendo el papel milimetrado, el espacio comprendido entre 2 líneas verticales, corresponderá por lo tanto, en la dimensión “TIEMPO” a 1/25 de segundo (0.04 segundo), o a 1/50 de segundo (0.02 segundo) según se desplace a 25 ó 50 mm x segundo respectivamente.
Además, el papel está milimetrado también horizontalmente y estando el galvanómetro calibrado de tal manera, que cuando recibe un potencial de 1 mili voltio (1 mv.), desplaza al sistema inscriptor 10 milímetros hacia arriba o hacia debajo de la línea isoeléctrica, tendremos que el espacio comprendido entre dos líneas horizontales (1 milímetro), representará la dimensión “INTENSIDAD” igual a 0.1 mili voltio.
La unidad ASHMAN es el espacio correspondiente a 1 milímetro cuadrado y representa a 2 dimensiones: Tiempo y Voltaje.
El tiempo está dado por la mensuración de líneas verticales dándose un valor de 0.04 seg. por cada una, si el papel rueda a 25 ms. x seg. en cambio, la dimensión Intensidad, que se mide en mV., está dada por los milímetros de desplazamiento del sistema inscriptor en sentido horizontal, hacia arriba o hacia debajo de la línea isoeléctrica, otorgándose el valor de 0.1 mV. por cada milímetro, cuando el equipo está calibrado a 1 cm = 1 mV. la intensidad de la corriente registrada por el equipo, está en relación directa con la proximidad del electrodo al corazón y sobre todo por el volumen de la masa muscular que la genera. De esta manera, un corazón voluminoso dará lugar a intensas corrientes y por tanto a amplios desplazamientos del sistema inscriptor.
Estandarización
Es la calibración del electrocardiógrafo en el factor “Intensidad”. La Estandarización se refiere a la respuesta del galvanómetro a la corriente recibida desde el amplificador, al cual, a su vez le llega desde el sistema de electrodos. Si el galvanómetro ordena al sistema inscriptor desplazarse en sentido vertical sobre la línea isoeléctrica 10 mm cuando le llega una corriente de 1 mV. de intensidad, la Estandarización es “-1-“. Pero, el electrocardiógrafo está en capacidad de aumentar más la señal eléctrica que le llega, en caso de que el corazón genere muy débiles potenciales, desplazando al doble los movimientos del sistema inscriptor, ante la entrada de 1 mV. de intensidad de corriente, o por lo contrario, si la masa muscular cardiaca produce corrientes muy intensas, que darían lugar a movimientos de la pluma inscriptora desde el borde superior al inferior del papel electrocardiográfico, como es el caso de los estados de Hipertrofia cardiaca de cualquier etiología, debemos reducir la respuesta al ingreso de corriente.
De esta manera podemos calibrar el equipo así:
Derivaciones Electrocardiográficas
El término “derivaciones” electrocardiográficas se refiere a los sitios de la superficie del cuerpo, donde se instalan los electrodos del electrocardiógrafo, para examinar la actividad eléctrica del corazón. Esta actividad eléctrica formada por las fases de despolarización y repolarización de cada una de las fibras musculares cardiacas, desarrolla un campo eléctrico en los tejidos circundantes, que son considerados en la electrocardiografía clínica como un medio conductivo relativamente homogéneo. Una derivación está integrada por 2 electrodos situados en la superficie corporal, entre los cuales, ante la actividad eléctrica cardiaca, se establece una diferencia de potencial, que es transmitida al amplificador y que será analizada por el galvanómetro. El término “derivación” se lo aplica también al trazado sobre el papel, obtenido por el par de electrodos localizados en cada sitio particular.
Las derivaciones electrocardiográficas examinan al corazón desde 2 planos perpendiculares entre sí: el plano frontal y el plano horizontal. El plano frontal explora la actividad eléctrica cardiaca mediante las derivaciones “estándar” y las derivaciones “unipolares de los miembros”. El plano horizontal explora el corazón mediante las derivaciones “precordiales”. Las derivaciones estándar son “bipolares”” y las unipolares de los miembros y precordiales son “unipolares”.
Representación esquemática de las derivaciones
Ubicación de las Derivaciones:
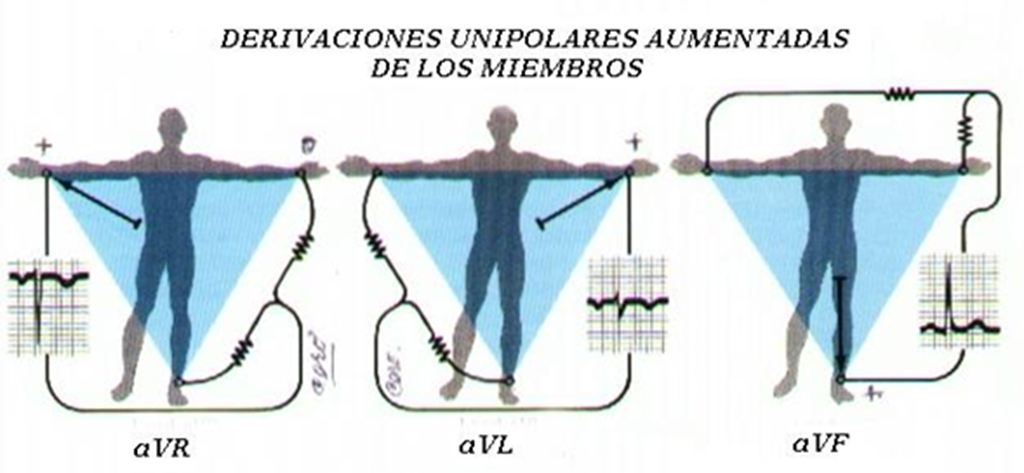
Las derivaciones unipolares de los miembros al contrario de las anteriores, cada una de ellas, representa el voltaje cardiaco captado en un determinado lugar del cuerpo con referencia a un punto no fluctuante (punto cero), conseguido mediante la conexión de los electrodos localizados en los restantes 3 miembros en una central terminal, cuyas conexiones se realizan automáticamente al mover el “dial” de control de las derivaciones en el tablero del electrocardiógrafo. El electrodo explorador (+) es el que, pareado con la central cero, capta el impulso eléctrico y lo transmite al amplificador.

Al igual que las derivaciones unipolares aumentadas de los miembros, las derivaciones precordiales trabajan con el electrodo (-) conectado a la central “cero”, mientras que el electrodo (+) ocupa diferentes posiciones sobre la superficie del tórax, que vamos a describir:
Estas derivaciones, si bien no proporcionan una visión de conjunto de la actividad eléctrica del corazón, en cambio por estar sumamente próximas a él, exploran con precisión las áreas sobre las que están proyectadas cada una de ellas.
Corte transversal del tórax. Nótese que la derivación V1 explora el ventrículo derecho; las derivaciones V2 y V3, la región del septum interventricular, las derivaciones V4 y V5, la región del ápex y la derivación V6, la pared libre de ventrículo izquierdo.
Derivaciones especiales:
En ciertos casos es necesario recurrir a otras derivaciones para explorar otras áreas del corazón o cuando el corazón ha sufrido un cierto grado de variación en su posición normal en el tórax:
La teoría del DIPOLO:
Un “dipolo” es un generador muy simple de cargas eléctricas, constituido por cargas de signo contrario, (+) y (-), separadas entre sí por una delgada placa, que en el caso de las células excítales se considera que es la membrana celular. Se acepta que en estado de “reposo”, la superficie exterior es positiva con respecto a la superficie interior que es negativa. Al ser estimulado un punto de la superficie exterior de la membrana, penetran a través de ella, hacia la superficie interior, cargas (+), iones de Ni-, que van a provocar una negatividad exterior (por pérdida de cargas +) que se va extendiendo progresivamente por toda la membrana celular; esto da lugar a una verdadera “onda” de despolarización, que siempre llevará una carga (+) en el frente y una carga (-) en la cola:
Estando los electrodos del electrocardiógrafo “mirando” la superficie exterior de la membrana celular cardiaca, transmitirán al galvanómetro una señal que será inscrita en forma de una onda por encima de la línea isoeléctrica, que llamaremos “onda positiva”. Una vez completada la despolarización y durante todo el tiempo que dure ella, no se captarán diferencias de potencial por parte de los electrodos, pues toda la superficie exterior de la membrana estará cargada de un solo signo que es el (-) y por tanto se inscribirá una línea horizontal que coincide con la línea isoeléctrica.
La repolarización comienza en el mismo sitio que comenzó la despolarización y se considera causada por la salida de iones de Potasio, que en resumidas cuentas van a llevar cargas positivas al exterior de la membrana, esto creará una “onda” que se irá extendiendo por la superficie exterior de la membrana, que llevará siempre una carga (-) al frente y una (+) en la cola:
Esta onda, al ser captada por los electrodos, dibujará una onda hacia abajo de la línea isoeléctrica, que se llamará “onda negativa”, por tanto la despolarización marcará una onda positiva y la re polarización dará lugar a una onda negativa:
Si la “onda” incide directamente sobre el electrodo explorador, lógicamente dará lugar a una onda inscrita de un tamaño mucho mayor a que si forma cierto ángulo con el electrodo, debido a que la captación será por supuesto menor.
Hasta el presente momento hemos considerado una sola fibra cardiaca, pero en el caso “in vivo”, los que captan los electrodos es un “resultante” de lo que sucede en todo el conjunto de fibras que forman el corazón.
Debemos tomar en cuenta además, que estructuralmente el corazón está formado por 2 masas sincitiales: la auricular y la ventricular, separadas por los anillos fibrosos de sustentación de las válvulas mitral y tricúspide, que darán lugar a ondas de despolarización y re polarización, individuales, de aurículas y ventrículos.
Sin embargo, en el perfil electrocardiográfico solo aparecen 3 ondas: la de despolarización auricular + la de despolarización ventricular + la de re polarización ventricular, pues la onda de re polarización auricular, por ser inscrita al mismo tiempo que comienza la despolarización ventricular, queda enmascarada por ésta, que tiene un voltaje superior y se impide su inscripción:
3.9.1 El perfil electrocardiográfico
3.9.2 Onda P
3.9.3 Espacio P-Q
3.9.4 Complejo QRS
3.9.5 Punto J
3.9.6 Complejo RS-T
3.9.7 Onda T
3.9.8 Onda U
El perfil o trazado del electrocardiograma no es igual para todas las 12 derivaciones del E.C.G. convencional. Si bien es cierto que el trazado puede ser parecido entre 2 derivaciones vecinas, por el contrario, si comparamos 2 derivaciones que estén muy alejadas una de la otra, los gráficos serán muy diferentes. Un ejemplo de ello es la enorme diferencia que existe entre a VR y D2; y entre V1 y V6, debido a la distancia de 180 grados que lo separa una de otra, en cada caso.
Es por este motivo, que si nos presentan un gráfico cualquiera y nos preguntan si es normal, debemos responder con otra pregunta. ¿A qué derivación corresponde el gráfico mostrado? ; Pues solo sabiendo en qué posición fue tomado el perfil que se nos muestra, podremos responder si es normal o no.
Los 2 gráficos de arriba y los 2 de abajo, son 4 trazados de las 12 derivaciones de un E.C.G. De reposo de la misma persona en estado normal; se escogieron los 4 trazados, para resaltar la diferencia entre las derivaciones opuestas.
Es necesario formarnos una idea de cómo debe ser el gráfico para cada una de las 12 derivaciones del E.C.G. convencional pues éste varia en la forma de inscribirse las ondas positivas o negativas, en altura y profundidad de ellas de acuerdo al ángulo de incidencia de la corriente sobre el electrodo explorador, si se aleja o se acerca a él y a la intensidad de la corriente generada por la masa muscular cardíaca subyacente. La comprensión de este último párrafo reviste tal importancia que se sugiere al lector revisar estos conceptos descritos.
Esta onda es producida por la despolarización de las aurículas; el vector resultante de la activación de cada una y todas al mismo tiempo de las células auriculares, nace a nivel del nódulo sinoauricular, en la cara posterior de la aurícula derecha, y se dirige de arriba hacia abajo, de atrás hacia adelante y de derecha a izquierda; por lo tanto, todas las derivaciones que sitúen su electrodo explorador en esta dirección van a “sentir” llegar la onda de despolarización y el galvanómetro marcará una onda positiva.
Pero, la derivación aVR, cuyo electrodo se encuentra a la derecha y arriba de las aurículas, graficará siempre una onda negativa. Esto significa que la onda P, producto de la despolarización auricular, normalmente debe ser positiva en la mayor parte de las derivaciones y debe ser, normalmente negativa en la derivación aVR.
En cuanto a la intensidad de la onda; debe tener una altura máxima de 2 mm, lo que significa un voltaje máximo de 0.2 mV.
La duración normal es también de 2 mm, que representa un tiempo de 0.08 seg., si el papel rueda a una velocidad de 25 mm. X seg.
Onda P en diferentes derivaciones:
Este espacio se mide desde el comienzo de la onda P hasta el comienzo de la onda “Q”, cuando existe onda Q.- Pero a veces, no existe onda Q por lo que se medirá hasta el comienzo de la onda “R”, en cuyo caso se llamará espacio “P-R”. Este espacio representa el tiempo que tarda el impulso nacido en el nódulo sino-auricular en despolarizar las aurículas + estimular las fibras de unión y excitar al nódulo aurículo-ventricular y aparecer en el haz de His.
En otras palabras, comprende el tiempo que toma el impulso nervioso cardíaco en estimular las aurículas, más el retraso normal que sufre el estímulo a nivel del nódulo A-V.
Mide normalmente 4 a 5 mm que representan 0.16 a 0.20 seg.en todas las derivaciones. La frecuencia cardíaca tiene cierta influencia sobre el espacio P-Q, pero no es muy marcada; en los niños la duración es menor, pero en los adultos tiende a aumentar posiblemente debido al envejecimiento celular normal que provoca menor velocidad de conducción.
El complejo QRS significa que el impulso eléctrico ha aparecido a nivel de la porción ventricular del haz de His y luego viajando por las porciones o ramas derecha e izquierda, ha despolarizado las masas ventriculares. En ciertas ocasiones puede faltar la onda Q, en cuyo caso será RS.- o puede graficarse solo la onda R, faltando la Q y la S. Finalmente puede faltar la onda R, denominándose entonces onda “QS”.
La activación ventricular no forma una onda simple, sino este complejo QRS, debido al complicada trayecto que sigue la onda de activación para conseguir la despolarización de los ventrículos.
Para poder comprender esto es necesario hacer uso de atención e imaginación por parte del lector: las 4 figuras que aparecen, representan 4 momentos diferente, desde que aparece el impulso nerviosos a nivel del haz de His; imaginemos que pudiéramos detener el impulso después de su iniciación, cuando han pasado: 0.01 – 0.02 – 0.04 y 0.06 seg. Desde su entrada a nivel ventricular.
Podríamos graficar las resultantes de las fuerzas electromotrices en forma de 4 “vectores” que tienen valores y trayectos diferentes. Imaginemos además que estamos tomando -al mismo tiempo- una derivación precordial derecha (V1) y una izquierda (V6)
Corresponde a la activación de la parte media y anterior del septum interventricular, es un vector de pequeño voltaje y se dirige desde la superficie izquierda del septum hacia la superficie derecha; es por tanto su dirección: de izquierda-derecha, de atrás-adelante y hacia arriba en los corazones verticales, como en las personas delgadas, o hacia abajo, en el corazón horizontal como en las personas obesas.
El electrodo situado en V1 sentirá aproximarse la onda de despolarización y marcará una pequeña deflexión positiva (onda R en V1), mientras que el electrodo localizado en V6 sentirá alejarse la onda y por lo tanto graficará una pequeña deflexión negativa (onda Q en V6).
IMPORTANTE: el primer vector es el que da origen a la onda R en V1 y a la onda Q en V6, de lo que deducimos que siempre habrá una pequeña onda Q en V6, pero no es normal encontrar onda Q en la derivación V1, si existe, será netamente patológica.
El lector deberá imaginar la influencia de este primer vector, sobre las derivaciones V2 – V3 – V4 y V5, que son intermedias entre las 2 posiciones examinadas, que van a graficarse deflexiones de acuerdo con el ángulo de aproximación o alejamiento, que forma el vector con la placa del electrodo explorador de cada una de estas derivaciones.
Cuando han transcurrido 0.02 seg de haber aparecido el estímulo en el haz de His, la resultante de las fuerzas electromotrices forman un vector dirigido de adelante-atrás, de derecha-izquierda y de arriba-abajo, o sea que la onda de activación está alcanzando la pared anterior de ambos ventrículos, cerca de la punta; el electrodo explorador localizado en V1, todavía sentirá acercarse la onda y se completará la onda R positiva en las precordiales derechas, en cambio el electrodo en posición V6 todavía sentirá alejarse de la onda y se completará la deflexión negativa (Q) de esta derivación.
Cuando ha transcurrido 0.04 seg., la onda de activación ha invadido la gruesa pared ventricular izquierda, desde la superficie endocárdica hacia la epicárdica, originando el más intenso de los vectores cardíacos, que se dirige de derecha-izquierda, de delante-atrás y hacia arriba en el corazón horizontal, o hacia abajo en el corazón vertical. Todos los electrodos correspondientes a derivaciones que se encuentran en la dirección de este vector, darán lugar a la inscripción de ondas positivas, de menor o mayor altura, de acuerdo al grado de incidencia del vector sobre el electrodo explorador; esto es especialmente cierto a nivel de las precordiales izquierdas y en D2, D3 y aVF. Desde una posición opuesta; la derivación V1, sentirá alejarse de la onda de activación y se formará una onda negativa (onda S), en ocasiones bastante profunda.
Las últimas regiones en despolarizarse son las partes posterosuperiores del tabique interventricular y las regiones basales cercanas a los anillos fibrosos de inserción de las válvulas mitral y tricúspide, que se consigue a las 0.06 seg.; el vector resultante se dirige de delante-atrás, de abajo-arriba y ligeramente hacia la derecha, dando lugar en V1 a la completación de la onda negativa “S” y el V6 se formará otra negativa “S” pequeña. La duración TOTAL de la QRS varía de 0.06 a 0.09 segundos.
Es punto de unión entre el final de la onda S y el inicio del segmento S-T; generalmente se encuentra al mismo nivel de la línea isoeléctrica, pero puede estar ligeramente desplazado hasta 1 mm. Hacia arriba o abajo.- Significa la terminación de la despolarización ventricular y el inicio de la repolarización.
Tiene un comienzo preciso: a nivel del punto J, pero su sitio de terminación es impreciso, debido al comienzo también impreciso de la onda T. Normalmente es horizontal e isoeléctrico, pero, puede sufrir un desnivel en cualquier dirección no mayor de 1mm. Eléctricamente corresponde a la “meseta” del potencial de acción de la membrana, la parte inicial de la re polarización. Cualquier injuria sobre la célula miocárdica, dará lugar a un desnivel de este segmento, y podrá observarse claramente, comparándolo con el nivel de la línea T-P (línea horizontal comprendida entre el final de la onda T y el comienzo de la onda P del nuevo ciclo), sin tomar en cuenta el nivel del espacio P-Q.
Se considera es producida por la parte final de la re polarización ventricular; es positiva en la mayor parte de derivaciones, con excepción de aVR en que es negativa y puede serlo también en las derivaciones precordiales derechas. Morfológicamente es asimétrica: con una primera rama menos vertical que la segunda; su cúspide o su cima, es redondeada. Una onda T simétrica y angular es muy probable que sea patológica, producida por trastornos de la re polarización ventricular.
Aclaración:
En una célula excitable aislada, la onda de re polarización se inscribe en sentido contrario a la onda de despolarización, por tanto, en la célula aislada, la onda T es siempre negativa.
Pero tomando en conjunto las células del corazón, la re polarización comienza en el sitio opuesto de donde comenzó la despolarización. La onda de activación ventricular se realiza desde el endocardio al pericardio; si la re polarización siguiera el mismo camino, la onda T normalmente sería negativa.
Pero posiblemente debido a grandes presiones que sufre la superficie endocardica, la re polarización comienza en sentido inverso, los electrodos de la piel captarán una onda T positiva.
Es una pequeña onda positiva, que se marca a veces a continuación de la onda T, especialmente en adolescentes y adultos jóvenes, pero su significación no está aún bien aclarada.
Consiste en un diagrama circular, en el que están representadas las derivaciones Standard y las Unipolares Aumentadas de los miembros, todas ellas esquematizadas en el plano Frontal.
El diagrama circular, está dividido en 2 mitades por una línea horizontal; Partiendo desde la derecha hacia arriba se mide en grados negativos (-) desde 0 a – 180 grados.
Así mismo, partiendo desde la derecha, se mide haca abajo en grados positivos (+) desde 0 a + 180 grados: es necesario memorizar el valor de cada una de las seis derivaciones representadas:
LA UTILIDAD DEL SISTEMA DOBLE TRIAXIAL DE BAYLEY: CÁLCULO RÁPIDO APROXIMADO DEL EJE ELÉCTRICO DEL CORAZÓN.-
El eje eléctrico de corazón representa la “resultante” de la suma algebraica de todas las fuerzas electromotrices generadas en el músculo cardíaco; su dirección se aproxima normalmente en el normo tipo, a los + 60 grados, pero se considera dentro de los límites normales, valores comprendidos entre los 0 grados y los + 90 grados.
El eje eléctrico –no necesariamente corresponde al eje anatómico del corazón- pues son dos materias algo diferentes.
Para calcular el eje eléctrico, se observan cuál de las Derivaciones Standard posee la onda “R” más alta; en principio, hacia ese valor en grados corresponderá al eje eléctrico.
Para afinar más el diagnóstico, observamos cuales son las vecinas de la elegida, tanto en las Standard como en las unipolares, pudiendo realizar una aproximación hacia arriba o hacia abajo del valor en grados del eje eléctrico.

Puede ocurrir el caso de que 2 derivaciones , que se encuentran en posición de “vecinas” en el gráfico del Doble Sistema Triaxial de Bayley, tengan ondas “R” del mismo tamaño; en este caso, el Eje eléctrico se encontrará equidistante de ellas.Ej.: Si encontramos ondas R iguales en D1 y en D2 (0 grados y +60 g.) Anotaremos el punto intermedio, o sea: Eje QRS= + 30 grados.- Otro ejemplo sería, si encontramos ondas R de igual altura en D1 (0 grados) y aVL (-30 grados); en este caso el eje QRS = – 15 grados.
La frecuencia de los latidos del corazón, puede ser calculada mediante el electrocardiograma conociendo previamente la velocidad de rodamiento del papel. En el electrocardiograma “convencional” o “estándar”, el papel se hace rodar a la velocidad de 25 mm. por segundo; por tanto cada mm. (Cada raya vertical) tendrá un valor de 4 centésimas de segundo (0.04 seg.). Luego, contamos la distancia en mm. que separa 2 ondas R en cualquier derivación; este valor lo multiplicamos x 0.04 = tiempo de duración, en centésimas de segundo de un ciclo cardíaco (sístole + diástole). Dividiendo 60 seg. para dicho tiempo, tendremos la Frecuencia cardíaca por minuto.
En el electrocardiograma mostrado arriba, la distancia entre 2 ondas R es de 18 mm.
Multiplicando: 18 mm x 0.04 seg = 0.72 seg.
1 minuto = 60 segundos
60 / 0.72 = 83
Frecuencia cardiaca = 83 x minuto.
3.10.1 Hemodinamia
3.10.2 Fórmula de presión arterial.
3.10.3 Relación entre presión—flujo—resistencia.
3.10.4 Concepto de resistencia periférica.
3.10.5 Efecto del hematocrito sobre la circulación.
3.10.6 .Concepto de presión sistólica—diastólica—media y diferencial.
3.10.7 Persistencia del conductor arterioso.
HEMODINAMIA
De acuerdo a las leyes de la Hemodinámica basadas en la física hidráulica, la presión dentro de un vaso sanguíneo es igual al flujo que circula por ese vaso multiplicado por la resistencia que oponen las paredes de los vasos a la circulación de la sangre.
Relación entre presión- flujo – resistencia:
P= F x R
El flujo es el contenido y las paredes del vaso sanguíneo el continente. En el caso de la fisiología sanguínea ambos factores pueden ser variables, analizaremos primero el flujo y luego la resistencia.
Fórmula de la presión arterial:
PA = GC x RP
PA= Presión arterial.
GC= Gasto cardiaco.
RP= Resistencia periférica.
Flujo.- es el gasto cardiaco por unidad de tiempo que se considera el minuto.
Gasto cardiaco.- es el producto de multiplicar el gasto sistólico por la frecuencia cardiaca por minuto.
GC= GS x FC
70mlx75 x m=5000ml.
FLUJO
Esto significa que en el normo tipo (individuo de género masculino 20 a 30 años de edad 1, 70 de estatura y 70 kg de peso. De buen estado de salud), en estado de reposo cada ventrículo inyecta en la arteria correspondiente 5000 ml de sangre por minuto.
La frecuencia cardiaca por minuto es la mayor determinante del flujo sanguíneo. Si la frecuencia cardiaca disminuye a menos de 60 x minuto la diástole se prolonga aumentando el volumen de fin de diástole y por tanto el volumen sistólico, es decir el volumen de sangre inyectada por cada ventrículo en su arteria correspondiente.
Esto es debido a la ley de Frank Starlyng, analizada en clases anteriores. Al aumentar el gasto sistólico aumentara el gasto cardiaco y aumentara la presión arterial.
Al contrario, si aumenta la frecuencia cardiaca por encima de 140 por minuto la diástole se acorta tanto que disminuye el volumen de fin de diástole, a consecuencia de que la sangre es tres veces más viscosa que el agua y necesita un tiempo determinado para poder pasar de aurículas a ventrículo. Si la frecuencia cardiaca es de 75 por minuto la diástole tendrá una duración de 50 cseg que es lo que requiere para completar el volumen de fin de diástole. Pero a una frecuencia de 140 x minuto la diástole será aproximadamente de 25 cseg, tiempo insuficiente para completar el llenado diastólico.
Con frecuencia superior a 140 por minuto el volumen de fin de diástole será progresivamente menor a medida que aumenta la frecuencia.
Si la frecuencia supera los 200 por minuto, el gasto cardiaco será tan pequeño que la persona se torna pálida, sudorosa y fría, pudiendo producirse pérdida del conocimiento por isquemia cerebral.
Isquemia significa disminución del riego sanguíneo a un órgano. No confundir con el termino infarto que significa obstrucción total del riego sanguíneo a un órgano.
RESISTENCIA PERIFÉRICA
El otro factor que influye sobre la presión sanguínea es la resistencia periférica.
La resistencia periférica está dada por el diámetro de las arteriolas. Arteriolas son vasos arteriales de menos de 100 micras de diámetro que tienen la característica de poseer abundante musculo liso inervado por el sistema nervioso simpático.
Al activarse el sistema nervioso simpático se contrae el musculo liso de las arteriolas disminuyendo su diámetro (vasoconstricción).
|
Lo contrario también es valedero: si aumenta el continente sin aumentar el contenido disminuye la presión arterial.
De todas formas cualquier aumento de la resistencia periférica determinara un aumento de la presión arterial. Una disminución de la resistencia periférica, disminuirá la presión arterial.
EFECTO DEL HEMATOCRITO SOBRE LA CIRCULACIÓN.
El hematocrito es él % del volumen sanguíneo que es ocupado por las células sanguíneas: glóbulos rojos, glóbulos blancos y plaquetas. Normalmente representan alrededor de 45%, ocupando el plasma sanguíneo el restante 55%.
De las 3 clases de células sanguíneas; los glóbulos rojos representan con mucha ventaja la mayor parte del hematocrito y solamente una muy pequeña parte glóbulos blancos y plaquetas.
De tal forma que la disminución de los glóbulos rojos significara obligatoriamente una disminución del hematocrito y un aumento compensatorio del volumen plasmático. La sangre será más fluida pero en cambio tendrá menor capacidad de transporte de O2. A medida que desciende el hematocrito el corazón aumenta la frecuencia de ahí el término taquicardia Sinusal compensatoria, característica de los estados que cursan con disminución del número de glóbulos rojos.
Por el contrario, el aumento de número de glóbulos rojos (poliglobulia) traerá como consecuencia un aumento del hematocrito, la sangre será más viscosa que lo normal, circulara lentamente por lugares estrechos por el exceso globular, con el peligro de que se active la vía intrínseca de la coagulación y la formación de trombos vasculares.
Trombo
Es una masa semisólida intravascular formada sin ruptura de la pared de los vasos sanguíneos.
Existen dos clases de trombos:
Trombos arteriales o trombos blancos: formados fundamentalmente por agregación plaquetaria. Estos trombos pueden prevenirse mediante la administración de antiagregantes plaquetarios como la aspirina (ácido acetil salicílico a bajas dosis).
La aspirina al penetrar en las plaquetas bloquea permanentemente a la ciclo oxigenasa, de tal manera que disminuye la formación de tromboxano A 2 que es el más potente proagregante plaquetario conocido.
Otro antiagregante plaquetario es el Clopidogrel que bloquea los receptores de ADP para que no se puedan unir las plaquetas y de esta manera disminuir la posibilidad de que se formen trombos arteriales
Trombos venosos: También llamados trombos rojos están formados fundamentalmente por una red de fibrina donde quedan atrapados abundante glóbulos rojos, por eso su color al microscopio de luz. Por supuesto que no responden a los antiagregantes plaquetarios, porque no es ese el mecanismo de formación. Para prevenir la formación de trombos venosos rojos se requiere la anticoagulación con Warfarina o con heparina.
CONCEPTO DE PRESIÓN SISTÓLICA
Presión sistólica es la fuerza que ejerce la sangre contra las paredes del vaso que lo contiene en el momento máximo del periodo de eyección. Ocurre cuando han trascurrido 15 Seg de la sístole ventricular (2 cseg+ 13 cseg que es la mitad del periodo de eyección) es por tanto muy fugaz.
CONCEPTO DE PRESIÓN DIASTÓLICA
Es la fuerza a que ejerce la sangre contra las paredes de las arterias mientras se encuentra cerrada la válvula aortica lo que representa toda la diástole (50 cseg si la frecuencia cardiaca es de 75 x min).
CONCEPTO DE PRESIÓN MEDIA
Teóricamente debería ser el resultado de la suma de presión sistólica + la presión diastólica y dividida para dos, pero es necesario tomar en cuenta el factor tiempo, por lo que la presión diastólica permanece más tiempo que la sistólica, por tanto si la presión sistólica es 120 y la diastólica fuera de 80, la presión media no estaría en 100 sino en alrededor de 92 mmHg.
CONCEPTO DE PRESIÓN DIFERENCIAL.
Es la resta aritmética entre la presión diastólica y la presión sistólica. Ps: 120 – Pd: 40 (mmHg) la presión diferencial es muy valiosa para ayudarnos a comprender ciertos trastornos que se pueden producir.
Si la presión diferencial disminuye a – 30 mmHg lo más probable que se trate de un estado de deshidratación, generalmente a causa de vómitos, diarreas o falta de ingestión de agua como en los casos de viajeros perdidos en zonas desérticas o sobrevivientes de naufragio en alta mar.
Por el contrario el aumento de la presión diferencial nos puede dar indicaciones, sobre todo de tres trastornos: arterioesclerosis, insuficiencia valvular aortica, persistencia del conducto arterioso.
La arterioesclerosis es un endurecimiento de las paredes arteriales por pérdida de su elasticidad: disminuye el continente, sin disminuir el contenido aumenta la presión arterial sobre todo la presión sistólica, ocurre frecuentemente a partir de la quinta década de la vida.
La Insuficiencia valvular aortica es otra trastorno que cursa con aumento de la presión diferencial. La causa es fundamentalmente un mal cerramiento de la válvula aórtica que es la que determina la presión diastólica. La insuficiencia valvular aortica por tanto aumentará la presión diferencial por disminución de la presión diastólica, un determinado volumen de sangre se regresa al ventrículo izquierdo y por tanto aumentará el volumen sistólico en la siguiente contracción, de modo que estará aumentada la presión sistólica, disminuida la presión diastólica y la presión diferencial se incrementara por ejemplo 140 sistólica 60 diastólica y presión diferencial 80 mmHg.
PERSISTENCIA DEL CONDUCTO ARTERIOSO
Es el ducto que comunica durante la vida intrauterina a la arteria pulmonar con el inicio de la aorta descendente. En ciertos neonatos este ducto persiste durante la vida extrauterina produciéndose el mismo efecto que en caso de la insuficiencia valvular aortica por el paso de sangre de la aorta hacia la arteria pulmonar con las consecuencias hemodinámicas esperadas: aumenta la presión sistólica y disminuye la presión diastólica aumentando la presión diferencial.
3.11.1 Músculo liso.
3.11.2 Pulsioximetro.
MÚSCULO LISO
La característica fundamental del musculo liso es que no tiene líneas Z por tanto al microscopio óptico no existe esa disposición regular de bandas claras y oscuras. Musculo liso si no hay líneas Z no hay sarcómera.
El músculo liso está distribuido en el sistema digestivo y en sistema vascular arterial, el músculo liso de las arteriolas que son vasos de menos de 100 micras de diámetro desempeñan un papel fundamental en la regulación de la presión arterial, cuando el músculo liso se contrae disminuye el diámetro de las arteriolas, aumenta la resistencia periférica y aumenta la presión arterial. El músculo liso de las arteriolas responde a la actividad simpática, que contrae las arteriolas de casi todo el organismo menos del músculo esquelético en el cual la actividad simpática las dilata.
El músculo liso no tiene túbulos T (túbulos transversos) y por tanto no tiene triada. Recordemos que el músculo esquelético tiene 2 triadas por sarcómera y el músculo cardiaco solamente una. Por eso el músculo esquelético tiene una contracción más rápida que el músculo cardiaco.
Tampoco el músculo liso tiene cisternas, porque su retículo sarcoplásmico es rudimentario y no está bien definido. Esta es la causa de que no tiene depósitos de calcio y su contracción depende del calcio extracelular.
Esto ha sido aprovechado por la industria farmacéutica para sintetizar sustancias que bloqueen los canales de entrada del calcio en el músculo liso de las arteriolas lo cual produce una dilatación y disminución de la resistencia periférica y de presión arterial.
Estos fármacos se denominan calcio antagonista y son de tres grupos:
1. Dihidropiridinas (Nifedipina)
2. Benzodiazepinas (Diltiazem)
3. Fenilalquilaminas (Verapamilo)
En el músculo liso los filamentos gruesos y filamentos delgados no están ordenados como en el músculo esquelético en el cual 6 filamentos delgados rodean a cada filamento grueso. Esto le da al músculo liso un mayor acortamiento de su longitud pues los filamentos delgados en cada contracción se interdigitan entre los filamentos gruesos, luego de unos segundos vuelven a acomodarse y se repite el ciclo nuevamente.
Entre las Dihidropiridinas anotamos:
La amlodipina es el fármaco más potente de este grupo y de mayor tiempo de acción, por este motivo puede administrarse cada 24 horas en forma segura.
En cambio la Nifedipina de acción corta a las 6 horas produce “picos” y “vallas” por lo que el laboratorio original tuvo que crear una forma farmacéutica de acción prolongada (Adalat Oros 20 – 30 y 60mg).
EL PULSIOXIMETRO
Es un dispositivo no invasivo que determina la Saturación de Oxígeno en la molécula de hemoglobina. Consiste en un rayo luminoso que se aplica en el lecho ungueal y determina el número de sitios ocupados por el oxígeno, en la molécula de hemoglobina que es transportada por los glóbulos rojos.
Debemos recordar que la sangre que abandona los capilares pulmonares sale saturada 100%, pero en el trayecto hacia la aurícula izquierda recibe la sangre proveniente de las venas bronquiales, por lo que su saturación desciende a 97%. Con esta saturación pasa al ventrículo izquierdo y luego a la aorta y sus ramas, por tanto el pulsioxímetro va a marcar en promedio 97%. En las enfermedades que cursan con escasa perfusión capilar pulmonar la saturación estará disminuida, lo mismo que en caso de hipoventilación alveolar.
Los pulsioximetros modernos transmiten la señal a un monitor donde se puede observar además del porcentaje de saturación, la frecuencia de pulso por minuto y la onda de pulso donde se puede observar la incisura dícrota por el cerramiento valvular aórtico, en la rama descendente de la onda de pulso.
3.12.1 Venas y sus funciones.
3.12.2 Presión venosa central.
3.12.3 El Sistema Linfático.
VENAS Y SUS FUNCIONES
Se llaman venas a los vasos sanguíneos que llevan la sangre al corazón. Son de paredes delgadas y poseen válvulas que son repliegues que tratan de evitar un flujo retrógrado, de manera que prácticamente la sangre es transportada casi pasivamente de una válvula a otra. Estando generalmente una arteria cerca de una vena, la onda de presión del pulso arterial o la contracción de un músculo esquelético, producen opresión de la vena y la sangre fluye en sentido anterógrado y no retrógrado, porque se lo impiden las válvulas, además, la función aspiradora del corazón contribuye a este efecto.
Las válvulas son repliegues de la íntima que hacen protrusión a la luz del vaso, que coaptan con pliegues idénticos que existen en la pared opuesta y que al cerrarse fraccionan la columna de sangre evitando su retroceso. Las vénulas son pequeños vasos que continúan a los capilares, pudiendo existir anastomosis con arteriolas, que cuando están permeables, pueden derivar la sangre arterial directamente a las venas sin pasar por los capilares.
Las venas tienen también la capacidad de crecer en ciertas circunstancias y de dilatarse cuando existe aumento de la presión interna.
Cuando aumenta la presión interna, las venas adoptan un trayecto serpenteante, que sería la disposición para atenuar la presión interna. Este estado se conoce con el nombre de várices.
Si se cortan 2 extremos de una vena y quedan libres, estos pueden anastomosarse nuevamente entre sí o desarrollar colaterales que da lugar a un verdadero puente entre los extremos venosos cortados. Este es el motivo por el que muchas veces, que a pesar de la extirpación quirúrgica de las várices, vuelven a formarse o sea que recidiva.
Las venas por convergencia sucesiva, forman 3 grandes troncos venosos que desembocan en la aurícula derecha: la vena cava superior, la vena cava inferior y el seno coronario.
| NOTA.- En el lado venoso no existe el homólogo de las arteriolas y de los esfínteres pre capilares. |
PRESIÓN VENOSA CENTRAL
Es un procedimiento invasivo, que sirve para medir la presión de la sangre en la aurícula derecha, de esta manera podemos analizar si el corazón está cumpliendo o no la ley de Frank-Stirling. Para realizarlo se introduce un delgado catéter desde la vena yugular o desde la subclavia hasta llegar a la aurícula derecha, luego se conecta el extremo proximal del catéter a un medidor de presión. Lo normal es entre 0 y 10 cm H20.
Si el corazón es insuficiente se acumula un gran volumen de sangre en las grandes venas lo cual aumenta la presión por encima de 10 en la aurícula derecha.
El tratamiento generalmente se basa en la administración de un diurético, por ejemplo furosemida con el objetivo de eliminar líquidos vía renal y secundariamente fármacos que aumenten la fuerza de contracción del corazón:
“Más vale quitarle carga a la carreta que darle fuete a un caballo cansado”.
En caso contrario cuando existe un estado de deshidratación, el valor puede marcar presión negativa, en cuyo caso debe administrarse líquidos. – Insertar grafico de PVC.
ELsSISTEMA LINFATICO.
Los capilares linfáticos periféricos son pequeños vasos de paredes extremadamente delgadas que nacen cerca de los capilares arteriales. Recogen un líquido llamado linfa que contiene una cantidad importante de proteínas plasmáticas, especialmente albúminas.
Luego confluyen por convergencia en vasos linfáticos de mayor calibre que tiene una distribución bastante particular: la mitad inferior del cuerpo y la zona izquierda de la mitad superior , incluyendo los capilares linfáticos provenientes de la circulación pulmonar, forman un gran vaso llamado conducto torácico que desemboca en la unión entre la vena subclavia izquierda y la yugular interna izquierda .
La mitad derecha de la parte superior del cuerpo reúne sus capilares linfáticos en la gran vena linfática derecha que deboca en la unión de la vena subclavia derecha con la yugular interna derecha.
De esta manera todo el contenido de la linfa, incluyendo su gran carga de proteínas se reintegra a la circulación.
En ciertas ocasiones, especialmente durante cirugías de tórax, puede lesionarse el conducto torácico y producirse una acumulación de linfa en la cavidad del tórax llamada quilotorax, la consecuencia sería la disminución de las proteínas plasmáticas estado muy peligroso, que debe corregirse con la administración (IV) de albúmina humana.
3.13.1 Circulación Capilar periférica
3.13.2 Difusión a través de la membrana capilar .
3.13.3 Fuerzas que determinan la circulación capilar periférica.
3.13.4 Concepto de edema y causas más comunes.
3.13.5 Tema especial: Fiebre reumática
CIRCULACIÓN CAPILAR PERIFÉRICA.
Los capilares son pequeños vasos situados entre la meta arteriola y la vénula, de paredes muy finas formadas por células endoteliales y membrana basal. Su número se calcula en varios cientos de millones y su superficie total entre 500 y 700 m.2. Las células se encuentran muy cerca, a no más de 20 o 30 micras de distancia.
DIFUSIÓN A TRAVÉS DE LA MEMBRANA CAPILAR.
Las sustancias como el O2 y el CO2 que son liposolubles, difunden directamente a través de la membrana capilar, en cambio las sustancias hidrosolubles, solo lo hacen a través de poros, que tienen un diámetro de 6 a 7 micras como la glucosa y los iones.
Es necesario explicar., que más adelante de las arteriolas, que son vasos de menos de 100 micras de diámetro, no existe presión sistólica y diastólica sino solo una presión única que es la presión hidrostática de la sangre.
FUERZAS QUE DETERMINAN LA CIRCULACIÓN CAPILAR PERIFÉRICA
Analizaremos la circulación capilar periférica, que tiene un comportamiento muy diferente a los capilares pulmonares, tema que será tratado en el capítulo 4 correspondiente a fisiología respiratoria.
Son 4 fuerzas que intervienen en el capilar periférico:
1. Presión hidrostática de la sangre: actúa de adentro hacia afuera, tratando de forzar la salida de líquido hacia el espacio pericapilar o intersticial. Su valor no es constante en toda la longitud del capilar, pues, en su extremo proximal o arterial es de alrededor de 30 mmHg, en cambio en el extremo distal o venoso, se calcula en 10 mmHg. La salida del líquido durante la longitud del capilar es la que produce la caída de la presión hidrostática.
2. Presión coloide osmótica de las proteínas plasmáticas. Se calcula que las proteínas plasmáticas ejercen una presión osmótica de 4 mmHg por cada gramo. Si la concentración normal es de 7 g x 100 ml de plasma, el total será de 28 mmHg, esta fuerza trata de retener líquido dentro del capilar oponiéndose a la presión hidrostática de la sangre.
En el extremo arterial, la presión hidrostática supera a la presión osmótica [ 30 VS 28) por tanto sale líquido al espacio intersticial. Pero en el extremo venoso, sucede lo contrario, la presión osmótica supera a la presión hidrostática ,28 vs 10, lo que da lugar a la entrada de líquido desde el espacio intersticial hacia el interior del capilar. Prácticamente todo el líquido que sale por el extremo arterial reingresa por el extremo venoso.
3. Presión de contacto del líquido intersticial. Se calcula en 6 mmHg, es la fuerza que ejerce el líquido intersticial sobre la superficie exterior de la pared del capilar. Se opone a la presión hidrostática.
4. Presión osmótica de las proteínas del líquido intersticial. Contiene una pequeña cantidad de proteínas, especialmente albuminas que se ha calculado en 1.5 g x 100 ml, lo que da lugar a una presión de 6 mmHg. Esta fuerza trata de retener líquido en el intersticio y se opone a la presión osmótica de la sangre capilar.
Debemos notar que las fuerzas # 3 y# 4 tienen valores similares, 6 mmHg, que actúan en sentido contrario y por tanto se anulan. Desde el punto de vista práctico, que salga o entre líquido en el capilar dependerá solo de las fuerzas #1 y #2.
EDEMA
En ciertas circunstancias, la cantidad de líquido que reingresa por el extremo venoso del capilar, es menor que la que salió por el extremo arterial. El líquido se acumula entre los capilares y las células estado patológico que se conoce con el nombre de edema.
Cuando es abundante se produce una depresión al presionar la piel, signo llamado fóvea. Si esto ocurre a nivel pulmonar, edema pulmonar, puede poner en peligro la vida del paciente por alterar la función respiratoria, como se estudiará en el cap. #4.
Causa del Edema: La principal causa de edema es la hipoproteinemia; La cantidad normal de proteínas en la sangre, es la encargada de evitar que se produzca edema al reintegrar a la circulación el líquido que salió por el extremo arterial del capilar.
Principales causas de hipoproteinemia
1. Desnutrición. Falta de proteínas en la alimentación.
2. Parasitosis intestinal, que consume las proteínas ingeridas.
3. Enfermedad renal. La membrana glomerular está formada de 3 capas como se verá en el cap. 5. La capa intermedia contiene proteoglicanos de carga negativa y como las proteínas tienen carga negativa, impide la salida de ellas por la orina .Algunas enfermedades lesionan esta capa de proteoglicanos permitiendo la perdida de proteínas y causando edema de origen renal.
4. Una enfermedad nueva recién identificada en los últimos tiempos, la enteropatía pierde proteínas, causada por estasis a nivel de la vena cava inferior puede dar lugar a hipoproteinemia por perdida de proteínas en las heces, causando edema generalizado.
En todos estos casos, el tratamiento consiste en eliminar el factor causante y la reposición mediante la administración de albumina humana en forma intravenosa.
TEMA ESPECIAL.-
FIEBRE REUMÁTICA.-
Es una enfermedad infecciosa producida por el Estreptococo Beta Hemolítico del Grupo A , que primero produce generalmente una faringitis. El organismo responde activando el sistema linfocitario especialmente Linfocitos TCD4 colaboradores los cuales destruyen al agente invasor.
Sin embargo, aún eliminados la actividad inmunológica persiste atacando a las válvulas cardíacas que parece que poseen grupos proteicos similares a los que poseen los Estreptococos Beta Hemolíticos. El resultado es la destrucción especialmente de las válvulas mitral y aórtica por trabajar a mayor presión, se pueden lesionar y perforar las ojuelas de la válvula aórtica dando lugar a una Insuficiencia valvular, lo cual disminuye la presión diastólica y por tanto la perfusión coronaria que depende a su vez de un buen cerramiento valvular . El peligro es grave pues a menor perfusión coronaria menor gasto cardíaco, lo cual trae menor perfusión coronaria, instalándose un sistema de retroalimentación positiva dañino para el organismo y que puede causar M.S.
La población infantil especialmente de género femenino entre los 9 y los 10 años de edad son susceptibles de adquirir la Faringitis Estreptocócica que muestra cierta benignidad pues requiere de varios años para lesionar las válvulas cardíacas (3-5 años), tiempo durante el cual puede prevenirse la afectación valvular y evitar una enfermedad catastrófica.
Es considerada una enfermedad autoinmune. El sistema inmunitario no reconoce lo propio de lo extraño. No hay datos de adquirir la Fiebre Reumática después de los 20 años de edad.
3.14.1 La circulación coronaria.
3.14.2 Anatomía funcional: coronaria derecha e izquierda
3.14.3 Regulación del riego coronario
3.14.4 Metabolismo energético del corazón.
3.14.5 La Placa de ateroma.
3.14.6 Concepto de cardiopatía isquémica.
LA CIRCULACIÓN CORONARIA
El corazón es el único órgano que se nutre así mismo, mediante dos arterias llamada coronaria derecha y coronaria izquierda. Estas arterias nacen distales a los senos de valsalva en la raíz aortica. La arteria coronaria izquierda se divide en dos ramas en la descendente anterior y la circunfleja, esta irriga la porción anterior y lateral del ventrículo izquierdo y la porción anterior del septum interventricular.
La arteria coronaria derecha emite una rama llamada descendente posterior y nutre en la mayor parte de las personas al ventrículo derecho y la parte posterior del ventrículo izquierdo.
La mayor parte de la sangre venosa del corazón se vierte a través del seno coronario en la aurícula derecha.
El riego sanguíneo coronario es de 0.7 a 0.8 por cada gramo de musculo cardiaco. Si un corazón normal pesa vacío alrededor de 250 a 275g esto representa 225ml de sangre por minuto o el 5% del gasto cardiaco.
El plexo coronario está formado por arterias coronarias epicardicas y arterias sub endorcadicas, desde las cuales se nutre el espesor del musculo cardiaco. El plexo sub endorcadico es más extenso que el subepicardico.
Regulación del riego coronario :El riego coronario está sujeto al ciclo cardiaco. Durante la sístole el riego coronario disminuye en todas las cavidades pero sobre todo en el ventrículo izquierdo en el cual la zona endocardica queda prácticamente sin flujo.
Durante la diástole se reanuda el flujo a nivel de todo el sistema coronario, otorgando una característica única en este órgano, contraria a lo que sucede en los demás órganos del cuerpo, en los cuales el flujo de sangre es mayor durante la sístole y desaparece durante la diástole. En el corazón es lo contrario disminuye durante la sístole y aumenta durante la diástole.
En estado de reposo, el musculo cardiaco extrae alrededor del 70% del contenido de oxigeno de la sangre coronaria, esto también contrasta con los órganos periféricos en los cuales solo es extraído el 30% en estado de reposo.
Esto tiene una implicación importante que debe ser analizada, porque en estado de actividad física extrema la sangre de las coronarias solo puede suministrar un 30% adicional de su contenido de oxígeno. Para poder suplir las necesidades de un musculo cardiaco en actividad extrema tiene obligatoriamente que aumentar el riego sanguíneo mediante un proceso de vasodilatación coronaria.
Se ha identificado a la adenosina como un potente vasodilatador coronario, probablemente liberada por el endotelio vascular ante la hipoxia, pero probablemente existan otros vasodilatadores de la coronaria que incluyen iones de potasio hidrogeno bradicinina y prostaglandinas
Pero las coronarias también reciben inervación del sistema nervioso autónomo simpático y parasimpático cuyos efectos directos se deben a la acción de neurotransmisores: acetil colina para el neumogástrico y noradrenalina para los nervios simpáticos. Debe notarse que la actividad parasimpática solo tiene un pequeño efecto de la dilatación de las coronarias, en cambio la inervación simpática es mucho más extensa. Los neurotransmisores noradrenalina y adrenalina deben unirse con receptores específicos alfa y beta. Los receptores alfa al ser estimulados producen vasoconstricción y los receptores beta al ser activados producen vasodilatación. Los vasos coronarios contienen ambos tipos de receptores.
METABOLISMO ENERGÉTICO DEL CORAZÓN
En condiciones de reposo, el musculo cardiaco utiliza ácidos grasos para obtener energía, en lugar de recurrir a los carbohidratos: el 70 % de su metabolismo normal proviene de ácidos grasos. Sin embargo, igual que en otros tejidos en situaciones anaeróbicas o isquémicas el metabolismo cardiaco puede recurrir a la glucolisis anaerobia para obtener energía, aunque obtiene poca cantidad con ello, en comparación con las grandes necesidades del corazón. Además, la glucolisis precisa de grandes cantidades de glucosa sanguínea y producen mucho ácido láctico, que constituyen probablemente una de las causas de dolor cardiaco en condiciones de isquemia. Igual que en otros tejidos, más del 95% de la energía metabólica liberada de los alimentos se utiliza para producir ATP en las mitocondrias. Este ATP suministra energía para las funciones celulares. En presencia de isquemia coronaria muy grave, el ATP se degrada ADP, AMP Y ADENOSINA.
Como la membrana es permeable a la adenosina, esta se pierde al pasar a la sangre circulante. Se cree que esta adenosina es la que induce vasodilatación de las arterias coronarias en situaciones de hipoxia, como ya comentamos. Sin embargo, la perdida de adenosina tiene una consecuencia celular grave. Cuando una isquemia coronaria intensa se prolonga entre media hora y una hora, como ocurre después de un infarto de miocardio o de un paro cardiaco, se pierde cerca de la mitad de adenosina de las células musculares cardiacas, y su sustitución por síntesis de nuevo no permite una reposion superior al 2% por cada hora. Por tanto, si persiste por media hora aproximadamente una isquemia grave, aunque luego desaparezca, puede ser tarde para salvar la vida de las células cardiacas. Casi con seguridad, es una de las principales causa muerte de las fibras miocárdicas a consecuencia de isquémia. También es una de las principales causas de la debilidad cardiaca que acompaña a las etapas finales del colapso circulatorio.
Es interesante observar que el corazón es un verdadero engúllelo todo, porque en actividad máxima es capaz de obtener energía en casi partes iguales de tres sustratos: ácidos grasos,glucosa e incluso ácido láctico. El ácido láctico, producto del metabolismo del musculo esquelético puede ser utilizado por el corazón como fuente de energía en un verdadero proceso de reciclaje metabólico.
LA PLACA DE ATEROMA
La placa de ateroma es una masa que contiene colesterol, calcio y células fibroticas que se desarrolla en el interior de las arterias. El término ateroesclerosis proviene de los vocablos griegos athero (“pasta”) y skleros (“duro, piedra”).
No proviene de arteros (“arteria”) .Mientras la placa que ocluye parcialmente una arteria se encuentre cubierta por un endotelio integro, solo ocasionara una disminución del flujo para el órgano afectado, termino conocido como isquemia. Pero si el endotelio se afecta por ejemplo con la presencia de radicales libres, productos del metabolismo alimenticio que requieren hidrogeniones, estos radicales libres lo toman de la membrana endotelial, lesionándola. Igual efecto tiene el humo de cigarrillo que puede lesionar el endotelio, poniendo en contacto al factor de von willebrand circulante con la colágena, se produce la adhesión plaquetaria (primera capa de plaquetas) y luego capas sucesivas (agregación plaquetaria) formándose el trombo que ocluye completamente la arteria: esto es lo que constituye el infarto del órgano. Por esta razón las antiagregantes plaquetarios como la aspirina a bajas dosis (81 mg) y el Clopidogrel 75 mg cada día son fármacos de primera elección en caso de diagnóstico presuntivo o definitivo de infarto agudo de miocardio.
3.15.1 Mecanismos reflejos a corto plazo de regulación de la presión arterial.
3.15.2 Reflejo preso receptor y quimiorreceptor
3.15.3 Reflejo isquémico del sistema nervioso central
MECANISMOS REFLEJOS A CORTO PLAZO DE REGULACIÓN DE LA PRESIÓN ARTERIAL
La regulación de la presión arterial es muy importante para mantener la homeostasis. Este término significa la preservación de las condiciones necesarias para el buen funcionamiento de los órganos. No es solo la presión arterial sino una serie de factores como la temperatura, frecuencia cardiaca frecuencia respiratoria, glucosa en sangre, electrolitos y muchos más, que se requieren mantener para conservar la homeostasis.
Para mantener la presión en sus niveles normales, sistólica 90 a 120 mmHg y diastólica entre 60 a 80 mmHg, existen varios reguladores que los hemos clasificados en mecanismos a corto plazo, mediano plazo, y largo plazo.
Los mecanismos a corto plazo, son reflejos que viajan a velocidad de las Motoneuronas, 140 mts x seg, por tanto pasan desapercibidos para la persona, que no se da cuenta generalmente que estos mecanismos están funcionando.
REFLEJO PRESO RECEPTOR
También llamado baro receptor. Se inicia mediante receptores de estiramiento que se localizan especialmente a nivel de cayado aórtico y en la bifurcación de las carótidas, los receptores del cayado aórtico cuando son distendidos por un aumento de la presión dentro de la arteria emiten señales inhibidoras al bulbo raquídeo vía X par craneal ( cardioneumogástrico), en cambio los receptores localizados en los cuerpos carotideos envían señales por el nervio de Hering, rama del glosofaríngeo, igualmente al bulbo, el cual responde inhibiendo al centro vasomotor y disminuye la actividad simpática vasoconstrictora normalizándose la presión arterial.
Este reflejo preso receptor normaliza la presión arterial cuando está alterada en un rango entre 60 y 180 mmHg de sistólica para nivelarla en alrededor de 120 mm.
Lo contrario es muy frecuente, cuando la presión arterial sistémica disminuye por el cambio de posición, los receptores aórticos y carotideos disminuye el número de impulsos inhibitorios hacia el bulbo, aumentando el centro vasomotor su actividad vasoconstrictora simpática elevando la presión arterial
Este reflejo funciona en todo momento que cambiamos de posición especialmente cuando de posición acostado pasamos a la posición de pie, la sangre por gravedad tendrá la tendencia a dirigirse hacia las zonas bajas del cuerpo, dejando al encéfalo con menos circulación, lo que podría producir mareos y hasta perdida del conocimiento por isquemia cerebral.
Pero si el reflejo preso receptor está en buenas condiciones, él se encarga de impedir la isquemia cerebral (hipotensión ortostatica) produciendo vasoconstricción de las partes inferiores del cuerpo, para que la sangre se distribuya por igual en todos los órganos, sin importar la posición de ellos.
Nos hacemos una pregunta, ¿por qué razón las personas mayores no es conveniente que se levanten bruscamente de su cama?
La respuesta seria que debido a la mayor edad de las personas las neuronas conducen a menor velocidad que lo que hacen normalmente en una persona de 20 a 30 años de edad. De esta manera no da tiempo a producirse el reflejo preso receptor inmediato sino que puede tardar unos cuantos segundos, por tanto producirse una isquemia cerebral, perdida del conocimiento, con el peligro de caídas y lo que es peor, fracturas Oseas.
Debemos recordar que la especie humana, a partir de los 35 años de edad comienza a perder progresivamente calcio del esqueleto, efecto más pronunciado en el género femenino que en el masculino y por tanto, en la 6ta década o más, se presenta osteoporosis en todos los géneros (pérdida de calcio de los huesos).
Parece ser que el depósito de calcio en los huesos se realiza hasta los 30 años de edad en ambos géneros, pero en relación directa con la actividad física. Debido a la tendencia de realizar menos actividad física, el género femenino deposita menos calcio en las 3 primeras décadas de la vida; cuando llegan a la 5ta o 6ta década tendrán mayor tendencia a las fracturas.
La administración de medicamentos depresores del sistema nervioso central tendrá un efecto negativo sobre la velocidad de conducción del reflejo preso receptor, por eso, debe tenerse cuidado en la administración de fármacos que depriman el sistema nervioso en las personas ancianas.
REFLEJO QUIMIORRECEPTOR
Los quimiorreceptores son células que responden sensiblemente a la hipoxia que se encuentran localizados en la bifurcación de las dos arterias carótidas primitivas pero también en el cayado aórtico.
Al ser estimulados por la hipoxia envían señales por los nervios de Hering-glosofaríngeo y por el nervio vago hacia el bulbo, además de la hipoxia, también los quimiorreceptores son estimulados por la consecuencia de ella: acumulación de (CO2) y de hidrogeniones.
La señal de los quimiorreceptores es transmitida al centro vasomotor y al centro respiratorio para aumentar la presión arterial, aumentar la frecuencia respiratoria y aumentar por tanto la po2 arterial. Este reflejo se activa cuando la presión sistólica es menor de 80 mmHg.
REFLEJO ISQUÉMICO DEL SISTEMA NERVIOSO CENTRAL
Cuando la presión sistólica se encuentra en niveles bajos, alrededor de 50mmHg se activa el llamado reflejo isquémico del sistema nervioso central. Con esta presión, el flujo sanguíneo es muy lento, se acumula anhídrido carbónico que se combina rápidamente con el agua del plasma de la siguiente manera:
C02 + H20 = C03H2 (ácido carbónico) el cual es muy inestable y se disocia rápidamente en C03H (bicarbonato) + H+ (hidrogeniones)
La presencia de hidrogeniones en los alrededores del centro vasomotor bulbar produce una potente estimulación simpática que produce constricción de las arteriolas periféricas, aumento de la resistencia y aumento de la presión arterial.
Pero este incremento de la presión arterial no puede ser mantenido en forma permanente sino alrededor de 10 min, tiempo durante el cual si la hipotensión es debida a una pérdida de sangre, debe ser compensada con administración de fluidos intravenosa o de lo contrario se producirá un shock cardiogenito irreversible. La normativa es clara si se ha perdido sangre debe reponerse con sangre. En la actualidad no se ha podido conseguir un sustituto sanguíneo que tenga las mismas características que la sangre humana, los bancos de sangre hasta el momento están en funcionamiento.
3.16.1 Mecanismos hormonales de regulación de presión arterial. Noradrenalina, adrenalina, renina, angiotensina, aldosterona.
3.16.2 La enzima convertidora de angiotensina y sus inhibidores.
3.16.3 Péptidos Natriuréticos.
Los mecanismos hormonales a diferencia de los mecanismos reflejos, actúan más lentamente, pues estas sustancias deben ser secretadas por las glándulas endocrinas, puestas en circulación y viajar por vía sanguínea hasta el tejido diana que es el órgano que debe realizar la función, viajando por tanto a velocidad de circulación de la sangre.
SISTEMA RENINA – ANGIOTENSINA – ALDOSTERONA.
Los riñones secretan renina ante varios estímulos:
1. Hipoxia, disminución de la p02 de la sangre
2. Disminución del sodio en el líquido tubular.
3. Disminución del flujo del líquido tubular.
La zona sensible a estos estímulos es el aparato yuxtaglomerular, situado entre las arteriolas aferente y eferente del glomérulo renal.
La renina puesta en circulación actúa sobre un sustrato que se encuentra libremente en la sangre, llamado angiotensinogeno que es un decapeptido, formado por 10 aminoácidos.
La renina escinde 2 aminoácidos del angiotensinogeno y lo convierte en un octapeptido llamado angiotensina 1 que no tiene propiedades vasoactivas.
La angiotensina 1, circula por la sangre y también por el espacio intersticial. Cuando pasa por los capilares pulmonares recibe la acción de la ECA plasmática (enzima convertidora de la angiotensina) y de la ECA tisular cuando circula por el hígado, corazón y cerebro.
En ambas situaciones, la angiotensina 1 pierde otro aminoácido y se convierte en un heptapeptido (7 aminoácidos) llamada angiotensina 2 que es una de las sustancias vasoconstrictora más potente que se conoce.
En 1980 se puso en el mercado internacional el primer inhibidor de la ECA cuya acción consiste en impedir que la angiotensina 1 se convierta en angiotensina 2, permaneciendo en forma inactiva, esta sustancia se conoce con el nombre captopril, y en los años siguientes siguieron apareciendo otras sustancias inhibidoras de la ECA de potencia igual o mayor que el captopril pero con un denominador común, todas terminan en el subfijo PRIL. Esto nos orienta sobre el efecto de estos fármacos terminados en Pril, que son inhibidores de la enzima convertidora de angiotensina.
Cuando se forma angiotensina 2, esta tiene 2 efectos, uno directo y otro indirecto.
Efecto directo de la angiotensina 2
Actúa por vía sanguínea sobre los receptores localizados a nivel del musculo liso de las arteriolas produciendo vasoconstricción, aumento de la resistencia periférica, y aumento de la presión arterial. Disminuye el continente sin disminuir el contenido.
Efecto indirecto de la angiotensina 2
Por vía sanguínea, la angiotensina 2 llega hasta las glándulas suprarrenales, donde actúa sobre la capa glomerular, la más externa de la corteza suprarrenal donde estimula la producción de aldosterona, el más potente mineralocorticoide de la corteza suprarrenal que también por vía sanguínea, actúa sobre el túbulo distal de la nefrona produciendo la reabsorción de sodio y agua y la eliminación de potasio o hidrogeniones de acuerdo a las necesidades del organismo.
Al reabsorberse el sodio y agua aumenta el volumen plasmático, aumenta el retorno venoso, aumenta el gasto cardiaco y aumenta la presión arterial.
Recordemos que la presión arterial es el producto de multiplicar el gasto cardiaco x la resistencia periférica, por tanto cualquiera de los dos factores que aumente también aumentara la presión arterial. La angiotensina 2 tiene doble efecto sobre la presión arterial pues aumenta ambos factores.
Efecto del exceso de aldosterona
Si por algún motivo la corteza suprarrenal produce un exceso de aldosterona, la consecuencia será una excesiva retención de Na y agua y una excesiva eliminación de K: hipernatremia con hipokalemia y tendencia a la hipertensión arterial.
Efectos de la disminución de la aldosterona.
Si por alguna lesión de la suprarrenal no se produce suficiente aldosterona, tendremos el efecto contrario: no se reabsorbe Na, se retiene K: Hiponatremia con Hiperkalemia, hipotensión arterial. Cuando el K supera los 7 mEq x litro se pone en peligro la vida por producirse paro cardiaco.
PEPTIDOS NATRIURÉTICOS
Péptido Natriurético Tipo B (mal llamado Cerebral/ Brain) es un polipéptido de 32 aminoácidos secretado por los ventrículos cardiacos en respuesta a la elongación de las fibras. Es secretado junto con un fragmento terminal inactivo de 76 aminoácidos, la prohormona N – Terminal (N-T pro BNP).
Su mecanismo de acción es disminuir la resistencia periférica y la Presión Venosa Central y además un aumentado de la Natriuresis.
Junto con el ANP (Péptido Natriurético Auricular) disminuyen el volumen sanguíneo y el Gasto Cardiaco.
Valores Normales: N-T pro BNP 125 picogramos x ml.
BNP 35 picogramos x ml.
Vida media N-T Pro BNP es de 1 a 2 horas.
BNP 20 minutos.
En caso de Insuficiencia Cardiaca el valor de BNP supera los 100 picogramos y el N-T pro BNP supera los 500 picogramos.
Valores inferiores a los normales descartan el diagnostico de Insuficiencia Cardiaca.
3.17.1 Los receptores de angiotensina y sus inhibidores
3.17.2 Papel del riñón en la regulación de la presión arterial
3.17.3 Concepto de la hipertensión arterial y su clasificación
LOS RECEPTORES DE ANGIOTENSINA Y SUS INHIBIDORES
El músculo liso de las arteriolas contiene receptores para la angiotensina 2 que provocan vaso constricción arteriolar. Estos receptores se conocen con el nombre de at 1.
Se han sintetizado sustancias que bloquean a estos receptores, llamados antagonistas de los receptores de angiotensina (ARA), que bloquean la unión entre angiotensina 2 y sus receptor especifico.
El primer compuesto sintetizado fue el Losartan, a partir del cual fueron creándose otros compuestos similares con mayor potencia que el Losartan. Pero todos tienen en común el subfijo sartan (valsartan, Irbesartan, telmisartan, candesartan y eprosartan)
Este grupo de antihipertensivos es uno de los más recientes sintetizados y parece que disminuye la proliferación del músculo liso arteriolar y disminución de la hipertrofia ventricular izquierda.
Pero tienen probablemente una desventaja con relación a los priles, los cuales impiden la producción de angiotensina 2, en cambio los sartanes no impiden su producción y pueden acumular angiotensina 2, lo que está bloqueada es su unión con su receptor y por tanto no hay vasoconstricción.
Otra aparente desventaja es que los ARA disminuyen la producción de aldosterona con lo cual disminuye la reabsorción de sodio(NA) pero también disminuye la eliminación de potasio (k) por vía renal por lo que se produce Hiperkalemia lo que puede ser muy peligroso para la actividad cardiaca.
PAPEL DEL RIÑÓN EN LA REGULACIÓN DE LA PRESIÓN ARTERIAL
El gran regulador finalmente de la presión arterial es el riñón que cuando está en buen estado de funcionamiento es capaz de normalizar tanto el volumen sanguíneo circulante que determina el gasto cardiaco, como de la cantidad de solutos osmóticamente activos, especialmente el contenido de sodio si se ha producido un aumenta de la ingestión de sodio que trae consigo un aumento del volumen plasmático y de la presión arterial.
La unidad funcional renal es capaz de aumentar la presión de filtración glomerular, disminuir la reabsorción de sodio aumentando el volumen de agua y sal eliminado por la orina, de esta manera, un aumento de la presión arterial, en el plazo de varias horas o pocos días regresa a su nivel normal.
Por el contrario si disminuye la presión arterial, por hipovolemia o hiponatremia, disminuye también la presión de filtración glomerular, se retiene sodio, se retiene agua y en el plazo de pocos días aumenta la presión hasta su nivel normal.
Debemos de recordar que el glomérulo tiene dos arteriolas una aferente y otra eferente, si se dilata la aferente, pero se cierra la eferente aumenta el flujo y la presión a nivel de los capilares glomerulares con lo cual se incrementa la presión de filtración glomerular y el volumen de ultra filtrado (orina primitiva) que dará lugar a un mayor volumen de orina definitiva que será expulsado al exterior de cuerpo.
CONCEPTO DE LA HIPERTENSIÓN ARTERIAL Y SU CLASIFICACIÓN
Hipertensión arterial es el aumento de la fuerza que ejerce la sangre contra las paredes de las arterias. Debemos de aclarar que cuando hablamos de presión arterial se supone que se trata de las arterias sistémicas ramas de la aorta. Porque también puede existir hipertensión arterial a nivel del sistema vascular pulmonar, con valores en mmHg muy diferentes en ambos casos.
Como existe presión sistólica y diastólica, el incremento de presión arterial puede ser sistólica, diastólica o lo más común que ambos valores estén aumentados.
Antiguamente se creía que era normal que los valores de presión arterial sistémica se van incrementando a medida que la persona aumentaba en edad.
Actualmente el concepto que prevalece es que la presión sistólica debe encontrarse entre 90 y 120 mmHg, la presión diastólica debe estar entre 60 y 80 mmHg, no importa la edad, género o raza en la especie humana.
3.18.1 La Endotelina y sus receptores
3.18.2 Vasopeptidasa neutra y sus inhibidores
3.18.3 Mecanismos de acción de los antihipertensivos
3.18.4 Reacción redox – radicales libres – antioxidantes.
3.18.5 Miocardiopatía no compactada.
3.18.6 Acción del simpático y parasimpático a nivel visceral.
LAS ENDOTELINAS Y SUS RECEPTORES
Son las sustancias probablemente vasoconstrictoras más potentes del organismo, que han sido identificadas por medio de cultivos de células endoteliales. Son en realidad un grupo de sustancias formadas por 3 compuestos relacionados.
Estos 3 compuestos de la Endotelina ofrecen una gran similitud estructural con la sarafotoxinas, que es una toxina obtenida del veneno de una serpiente (actractaspis-engaddensis), cuya mordedura ocasiona la muerte como resultado de isquemia miocárdica debido a espasmos de las arterias coronarias.
La Endotelina (ET-1) es un potente vasoconstrictor y estimulante del crecimiento del musculo liso, es sintetizada por el endotelio vascular en respuesta a una serie de factores como la angiotensina II y la insulina.
La Endotelina no es almacenada en grumos, sino que es sintetizada y excretada inmediatamente ante ciertos estímulos:
1. Hipoxia tisular
2. Presencia de adrenalina
3. Trombina y angiotensina II.
Receptores de ET-1
Es un receptor ligado a las proteínas G (en la membrana) que al recibir al agonista, generan IP3, DAG, y sobre todo aumento del calcio iónico intracelular, que son segundos mensajeros que van a realizar el efecto esperado.
Existe otro receptor ET-B que se encuentra en las células endoteliales el cual produce liberación de óxido nítrico y prostaciclina que son 2 sustancias con efecto vasodilatador.
Por tanto la Endotelina I tendría un efecto bifásico: vasoconstrictor y vasodilatador, pero el mecanismo de esta relación no está suficientemente aclarado.
La Endotelina I se deriva de la preproendotelina que luego es convertida en proendotelina y luego se transforma en Endotelina por la enzima convertidora de Endotelina (ECE), una metaloproteinasa neutra que no circula en el torrente sanguíneo, la angiotensina II parece activar todo este proceso a nivel de la célula endotelial, la Endotelina formada va a actuar a través de receptores específicos a nivel del musculo liso arteriolar y en las glándulas suprarrenales. Estos receptores pueden ser inhibidos por un fármaco llamado bosentan que actualmente no está disponible en Ecuador por su elevado costo.
VASOPEPTIDASA NEUTRA Y SUS INHIBIDORES
La vasopeptidasa neutra es una enzima que degrada al péptido natri urético auricular que es un poli péptido con efecto vasodilatador liberado por las células musculares de las aurículas, como respuesta al aumento del volumen circulatorio y de la presión arterial. Su efecto se realiza a nivel del riñón donde produce dilatación de las arteriolas aferentes y constricción de la arteriola eferente con el consiguiente aumento con la presión de filtración glomerular y la eliminación de mayor volumen de orina.
El Omapatrilato es una sustancia con propiedades inhibitorias de la vasopeptidasa neutra y de la enzima convertidora de angiotensina (ECA), se inhibe al Inhibidor: el péptido natriurético auricular puede actuar.
Al inhibir a la Vasopeptidasa se produce una disminución en la presión de fin de diástole del ventrículo izquierdo, disminución de la resistencia vascular periférica acompañados de un incremento del gasto cardiaco.
MECANISMOS DE ACCIÓN DE LOS ANTIHIPERTENSIVOS
Hasta el momento se han podido sintetizar fármacos antihipertensivos con diferentes mecanismos de acción como son los siguientes:
1. Calcio antagonistas. Impiden la entrada del calcio a la sarcomera.
El músculo liso de las arteriolas, al igual que el de otros órganos, dependen para su contracción del calcio extracelular, porque su retículo sarcoplasmático no tiene cisternas. Esto las diferencia al musculo liso del musculo estriado presente en músculo esquelético y corazón , que no dependen del calcio extracelular pues tienen cisternas que acumulan con calcio en sus sarcomeras.
Existen 3 grupos de fármacos antagonistas del los canales del calcio:
Dihidropiridinas: Nifedipina -Amlodipina
Fenilalquilaminas: Verapamilo
Benzotiacepinas: Diltiazem
Sus efectos secundarios mas importantes son: edema maleolar- parálisis intestinal y dificultad para eliminar orina.
La Nifedipina se usa en Obstetricia para detener la contracción uterina en caso de amenaza de parto prematuro. Realizan el efecto contrario del Betabloqueador no Cardioselectivo que aumentan las contracciones uterinas.
Calcio antagonistas. Impiden la entrada del calcio a la sarcomera.
El músculo liso de las arteriolas, al igual que el de otros órganos, dependen para su contracción del calcio extracelular, porque su retículo sarcoplasmático no tiene cisternas. Esto las diferencia al musculo liso del musculo estriado presente en músculo esquelético y corazón, que no dependen del calcio extracelular pues tienen cisternas que acumulan con calcio en sus sarcomeras.
Existen 3 grupos de fármacos antagonistas del los canales del calcio:
Dihidropiridinas: Nifedipina -Amlodipina
Fenilalquilaminas: Verapamilo
Benzotiacepinas: Diltiazem
Sus efectos secundarios mas importantes son: edema maleolar- parálisis intestinal y dificultad para eliminar orina.
La Nifedipina se usa en Obstetricia para detener la contracción uterina en caso de amenaza de parto prematuro. Realizan el efecto contrario del Betabloqueador no Cardioselectivo que aumentan las contracciones uterinas.
2. Betabloqueadores. – Fueron unos de los primeros antihipertensivos producidos por la industria farmacéutica.
Pero existen por lo menos 2 tipos de receptores beta que aceptan a las catecolaminas ejerciendo una acción simpático nimetica : Receptores beta 1 y Receptores beta 2
Los beta 1 predominan a nivel del corazón.
Y su estimulación aumenta las 5 propiedades cardiacas.
En cambio los receptores beta 2 predominan a nivel de bronquios, hígado y músculo uterino. Su estimulación produce broncodilatación y relajación uterina. A nivel hepático promueven la formación de glucógeno a partir de sustancias que no son carbohidratos.
El bloqueo de estos receptores dará lugar a: diminución de la fuerza de contracción y frecuencia cardiaca, pero también a broncoconstricción (Contraindicados en los procesos bronquiales), contracción del útero gravídico (Contraindicados en los casos de amenaza de partos prematuros) y en algunos casos hipoglicemia severa por disminución de la gluconeogénesis y por tanto de la disponibilidad de glucosa para el mantenimiento de los procesos energéticos.
El mas conocido es Propranolol pero su utilización como antihipertensivo ha disminuido actualmente por los efectos secundarios mencionados.
Actualmente existen betabloqueadores cardio selectivos que solo actúan a nivel de los receptores beta 1 cardiacos, aunque administrados a altas dosis tienden a perder su cardio selectividad: Atenolol / Metoprolol/ Bisopronol y Nevibolol
3. Inhibidores de la renina plasmática: si no hay renina no habrá angiotensina, disminuye el gasto cardiaco y la resistencia periférica. Es un fármaco bastante nuevo y se llama aliskiren.
4. Inhibidores de la Enzima Convertidora de Angiotensina (IECA): Fueron comercializados a nivel mundial a partir de 1980.- La Angiotensina 1, un decapéptido, es inactiva , para ejercer su acción vasoconstrictora debe ser transformada en Angiotensina2, un Octapeptido, mediante la acción de la enzima convertidora; esto se realiza especialmente a nivel de la circulación pulmonar capilar, pero también puede realizarse mediante una enzima similar a nivel de hígado, riñón y cerebro.
Si se inhibe esta enzima, no se realizara la conversión de Angiotensina 1 en angiotensina 2, con lo cual el sistema Renina – Angiotensina- Aldosterona se interrumpe, dando lugar a vasodilatación arteriolar y eliminación de Sodio y agua, lo cual es beneficioso para el tratamiento de la Hipertensión arterial sistémica, pero se detiene la eliminación de potasio, pues, bloqueada la producción de aldosterona por no existir Angiotensina 2, no se reabsorbe sodio en la Nefrona, pero tampoco se elimina Potasio, el cual puede acumularse peligrosamente.
Se dice que el primer síntoma de la Hiperkalemina, es la muerte súbita. Esta enzima también se encarga de metabolizar a la bradicinina, que al acumularse es la responsable del efecto secundario mas importante de estos fármacos: La Tos.
El primero fue el Enalapril, siguiendo después una serie de fármacos todos terminados en PRIL, si uno de ellos produce Tos, todos los demás terminados en PRIL , también producirán este efecto secundario. Actualmente el Enalapril solo se utiliza en casos de Insuficiencia Cardiaca a dosis muy baja, 5mg c/dia.
5.-Antagonistas de los receptores de angiotensina.- Para poder ejercer su acción vasoconstrictora, la angiotensina 2 (de 7 aminoácidos) debe unirse a su receptor especifico. Los antagonistas ocupan su receptor y por tanto la angiotensina no puede producir vasoconstricción ni estimular la producción de aldosterona, por parte de la capa glomerular de la corteza de las suprarrenales. Por este motivo estos fármacos dan lugar a vasodilatación arteriolar y eliminación de sodio por vía renal.
El primero en ser sintetizado fue el Losartan, en el la década de 1990, pero actualmente existen en el mercado mundial Valsartan-Telmisartan- Candesartan- Irbesartan- Olmesartan, y otros, todos terminados en sartan.
Nótese que los inhibidores de la renina, los inhibidores ECA y los antagonistas de los receptores de angiotensina disminuyen la producción de aldosterona, con lo cual disminuye el sodio plasmático y aumenta el potasio, peligro de hiperkalemia.
6. Diuréticos: son sustancias que aumentan la producción del volumen urinario con lo cual se elimina líquido pero también sodio y potasio. Disminuyen el volumen plasmático y por tanto reducen la presión arterial Furosemida – HCT – Espironolactona.
La Furosemida actúa a nivel de la porción gruesa de la rama ascendente del ASA de Hente, impide la resorcíon de Sodio, el cual continua por los túbulos y se elimina con gran volumen de agua. La toma de una tableta de 40 mgs. Tiene una acción de 3 a 4 horas. La ampolla de 20mgs para uso intravenoso inicia su acción en 15 minutos y se lo utiliza para tratar emergencias hipertensivas.
La Hidroclorotiazida (HCT) y la Clortalidona, actúan a nivel del Tubulo Distal, eliminan Sodio, pero también Potasio. La HCT tiene 3 horas de acción, pero la Clortalidona 24 horas. ambas se presentan en tabletas de 25mgs.
La Espironolactona, antigua, y la reciente Esplerenona, Antagonizan a la Aldosterona. Esta hormona mineralo corticoide intercambia Sodio, el cual retiene junto con agua y elimina Potasio. Si se antagoniza su acción se produce el efecto contrario. la retención de Potasio puede ser peligrosa. Actualmente se la administra para el tratamiento de la Insuficiencia cardíaca.
Tabletas de 25 mgs.
7. Antagonistas de los receptores de endotelina: es la consecuencia de la acción de la angiotensina 2 sobre el endotelio, al sintetizar endotelina, esta actúa sobre el musculo liso produciendo vasoconstricción. Si se inhiben estos receptores se producirá el efecto contrario. El fármaco actualmente disponible es el bosentan. Actualmente muy caro.
8. Inhibidores de la vasopeptidasa neutra: el fármaco se conoce con el nombre de omapatrilato. Si se inhibe la vasopeptidasa neutra, no hay quien inhiba al péptido natri urético auricular y este puede ejercer su función a nivel renal, eliminando sodio, por más tiempo.
Sin embargo el Omapatrilato actualmente no ha sido aprobado por el servicio de salud de algunos países, probablemente por producir edema angioneurotico.
Recientemente, se encuentra en el mercado Internacional de fármacos SACUBITRIL (LCZ696) que inhibe a la Neprilisina, que es una Vasopeptidasa que a su vez inhibe al péptido natriurético.
El resultado final es inhibir al inhibidor, por lo que el péptido natriurético actua como antihipertensivo.
9. Vasodilatadores directos, mediante el bloqueo de los receptores alfa-1. Actualmente de uso restringido por presentarse frecuentemente hipotensión al cambio de posición, especialmente por la mañana. , los que más se han usado son la doxazosina y la terazosina, que tienen una aplicación en la hiperplasia benigna prostática.
10. Estimulantes de los receptores Alfa-2 adrenérgicos (alfametildopa) su mecanismo de acción es estimulando la captación de noradrenalina por los receptores alfa-2 presinápticos.
Su escasa potencia de acción, ampliamente superado por antihipertensivos más potentes lo ha llevado a salir recientemente del mercado
11. Nitrioprusiato de sodio.- es un potente vasodilatador arterial y venoso su uso es exclusivamente en forma de infusión intravenosa, en pacientes no ambulatorios sino en la unidad de cuidados coronarios
Su presentación es en frascos de 50mgs, la dosis entre 0.2 a 6.0 microgramos por kg de peso por minuto.
Se recomienda iniciar con 0.5microgramos por kg de peso por minuto, si se diluyen los 50mg en 250ml de dextrosa al 5%, cada ml contendrá 200 microgramos de nitrioprusiato para una persona de 70kg de peso, se tendrá que administrar en bomba de infusión continua 10ml por hora para de esta manera cubrir su necesidad inicial, en cuanto a disminución de la presión arterial, pudiendo incrementarse de acuerdo a la respuesta que se presenta.
Como ejemplo para un paciente de 70kg:
0.5 x 70 kg x 60 minutos = 2100 microgramos x hora.
Si se diluyen 50 mg en 250ml de dextrosa al 5%, tendría que realizarse la siguiente regla de 3
Se requiere una dosis de 2100 microgramos x hora, dividimos esta cifra para 200, y da una cifra de 10.5ml x hora como dosis inicial
Es probable que en un futuro se sinteticen otras sustancias antihipertensivas con diferentes mecanismos de acción, o que se combinen en un solo comprimido 4 o 5 o más fármacos con diferentes mecanismos.
La tendencia actual es combinar varios fármacos a bajas dosis para minimizar los efectos secundarios que aparecen cuando se lo administran a altas dosis
12. Fenoldopan:_Es un fármaco utilizado en emergencias hipertensivas. Es un estimulador de los receptores D A1 de la dopamina, de uso intravenoso, es vasodilatador arterial de las coronarias, renal y mesentéricas, y a demás tiene efecto diurético.
Esta aprobado por la FDA para el tratamiento de la HTA sistémica severa con pacientes hospitalizados. Su efecto es rápido y rápidamente reversible.
Es de mucha utilidad en los hipertensos con insuficiencia renal, por estimular los receptores de dopamina en los túbulos de la nefrona, con lo que se estimula la excreción de sodio.
Se diferencia de la dopamina, porque solo estimula los receptores D1, sin efecto sobre los receptores alfa o beta como si lo hace la dopamina.
Fenoldopan es el único agente intravenoso disponible, que disminuye la presión arterial sistémica y al mismo tiempo mejora la perfusión renal.
Causa taquicardia dosis dependiente y puede causar aumento de la presión intra ocular por lo que está contraindicado en casos de glaucoma.
Dosis 0.1microgramo por kilogramo por minuto.
Su acción es parecida al nitrioprusiato de sodio pero no causa intoxicación por cianuro.
También llamada reacción de oxido- reducción en que intervienen dos agentes:
Uno llamado oxidante y otro llamado reductor. El agente oxidante capta electrones de otra estructura, de tal forma que el mismo queda en un estado menor de oxidación de la que tenía, por esto se dice que queda reducido .
En cambio el agente reductor que suministra los electrones, incrementa su estado de oxidación al ceder sus electrones y se torna más oxidado que antes de la reducción..
RADICALES LIBRES.-
Los radicales libres son átomos o grupos de átomos que tienen necesidad de captar un electrón de las moléculas que conforman el endotelio Los radicales libres son producto del metabolismo del propio organismo pero pueden verse incrementados en ciertos estados como la exposición repetida a hidrocarburos aromáticos como el humo del cigarrillo y el consumo de ácidos grasos de origen animal.
Los radicales libres al tomar electrones de otras estructuras, quedan reducidos, pero la estructura afectada queda oxidada.
LOS ANTIOXIDANTES.-
La administración de ciertas sustancias naturales como la vitamina c , la vitamina e, el ácido omega3 y otros productos llamados antioxidantes, tendrían la capacidad de dar al radical libre el electrón que andan buscando, de esta forma el endotelio vascular no sufriría daño alguno .
Podríamos decir que el antioxidante le da de comer al “perro hambriento” , para que deje tranquilo a nuestro endotelio.
El endotelio vascular cuando, es afectado por los radicales libres, disminuye la capacidad de producción de prostaciclina óxido nítrico , agentes vasodilatadores, con lo que predominan los agentes vasoconstrictores,tromboxano A-2 , las endotelinas. Además la lesión endotelial, podría poner en contacto la colágena subendotelial y las plaquetas , desarrollando trombos intravasculares .
Terminología:
Dona electrones a otra molécula, en la cual se produce una reducción, pero el mismo queda oxidado.
Ejemplo Vitaminas C y E.- Coenzima Q10.
MIOCARDIOPATÍA NO COMPACTADA
También llamada Miocardiopatía descompactada o Miocardiopatía Hipertrabeculada. Es una patología recientemente identificada, debido al progreso de la ecocardiografía Bi y Tridimensional. Consiste en la presencia de trabeculas a nivel de ventrículo izquierdo que pueden dar lugar a un espacio no compacto entre el endocardio y el miocardio por la presencia de formaciones trabeculares de más de 10mm de longitud.
Se considera que es de origen genético, encontrándose grupos familiares que presentan esta anomalía.
Se considera que existe el peligro de producirse tromboembolismo sistémico y que pueden ser el origen de arritmias ventriculares graves. Hasta el momento no existen criterios bien establecidos para su diagnostico.
Sistema Renina Angiotensina Aldosterona : la Renina es una enzima liberada por el aparato yuxtaglomerular en respuesta a:
a) Hipotension
b) Bajo flujo de sodio en el glomerulo
c) Hipoxia.
La Renina circulante actua sobre una proteina llamada llamado Angiotensinogeno producida en el higado, al cual convierte por eliminacion de aminoacidos en Angiotensina I, que no tiene efectos vasomotores.
Al circular por los capilares pulmonares sufre la accion de una vasopeptidasa llamada enzima convertora de angiotensina que transforma a la angiotensina I en angitensina II la cual tiene un efecto vasoconstrictor potente de las arteriolas la ECA no solo se encuentra en los capilares pulmonares sino tambien en algunos tejidos como higado, corazon y cerebro (ECA plasmatica- ECA tisular ).
La angiotensina II actua a nivel de las arteriolas produciendo vasoconstriccion, disminucion del diametro, aumento de la resistencia periferica y aumento de la presion arterial, siendo este un efecto directo de la angiotensina II.
Pero tiene tambien un efecto indirecto: actuando sobre la capa glomerular ( externa ) de la corteza suprarrenal estimula la produccion de aldosterona que por via sanguinea llega al tubulo distal de la nefrona produciendo retencion de sodio y agua con lo que aumenta el volumen plasmatico, el gasto cardiaco y la presion arterial. La absorcion de sodio se acompañia con eliminacion de potasio o hidrogeniones de acuerdo a las necesidades del organismo.
Por tanto la angiotensina II eleva la presion por 2 mecanismos:
Directo: vasoconstrictor.
Indirecto : retencion de sodio y agua